Les TOPS 5 ADA 2023 en diabétologie
Dr Laurent Meyer
TOP 5 – L’annonce précise des glucides aux repas n’est plus une condition essentielle au bon résultat de la boucle fermée, ça se confirme
Parmi les conditions actuelles de mise en place d’une boucle fermée dans le diabète de type 1 (DT1), la capacité du patient à évaluer les quantités de glucides ingérés aux repas tient une place prépondérante. Outre le fait que cette évaluation n’est guère facile malgré de nombreux outils mis à disposition des patients, cette tâche rébarbative se heurte rapidement à la lassitude des patients au fil du temps, constituant un véritable fardeau pour la plupart d’entre eux. Dans un article paru dans la revue Diabetes Care début 2023 (1), une équipe diabétologique du Qatar avait étudié l’effet du compte précis des glucides alimentaires versus une quantité fixe, calculée individuellement, sur la qualité de l’équilibre glycémique obtenu chez des adolescents vivant avec un DT1 traité avec le système Minimed™ 780G. Cet essai prospectif randomisé de 12 semaines incluant 34 patients avait permis de montrer qu’une annonce fixe de glucides aux repas permettait d’atteindre les objectifs internationaux, constituant ainsi une alternative envisageable au compte précis.
L’étude d’extension à 6 mois
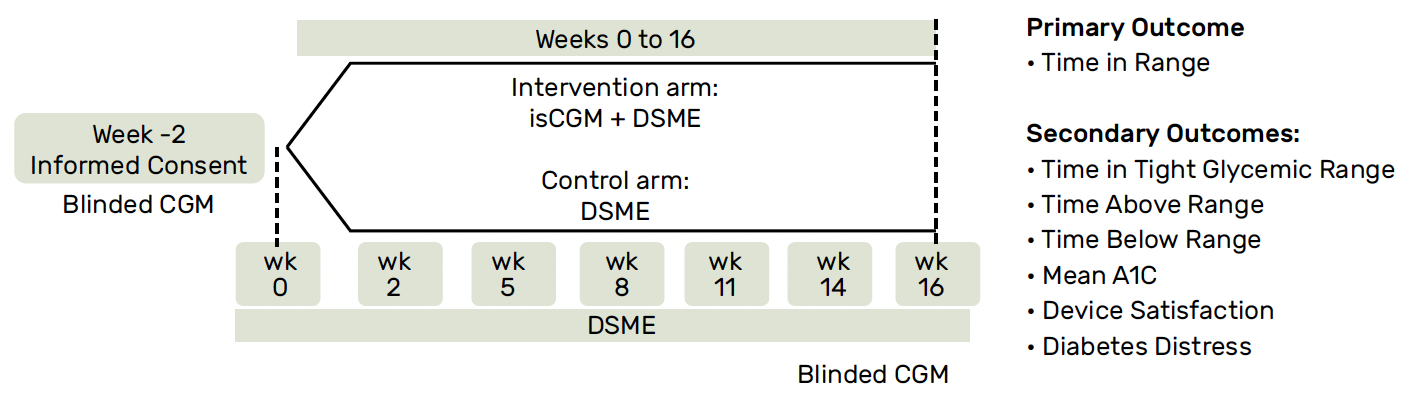
Les résultats de l’étude d’extension à 6 mois ont été présentés par Goran Petrovski au cours du dernier congrès de l’ADA. Dans ce travail, dont la méthodologie est résumée dans la figure 1, la population étudiée poursuivait l’approche initiale de 12 semaines permettant d’observer les effets à 6 mois d’un compte précis de glucides alimentaires versus une quantité fixe individualisée.
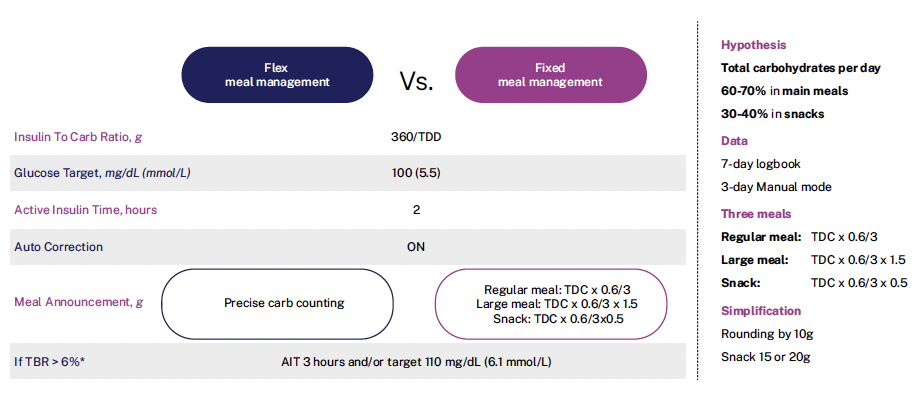
Figure 1 – Méthodologie de l’étude d’extension à 6 mois.
Les résultats
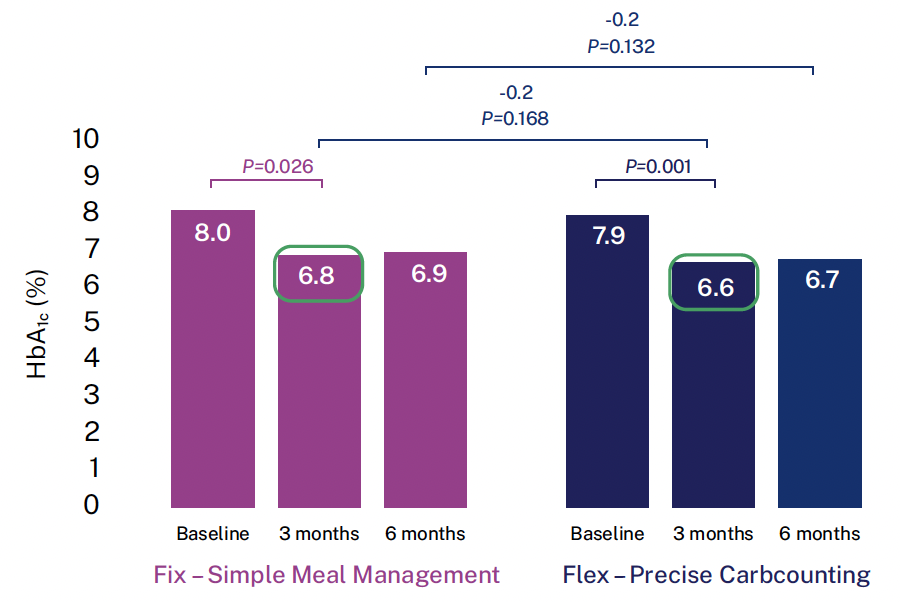
Les résultats à 6 mois concernant l’évolution de l’HbA1c sont rassurants, permettant d’objectiver une baisse significative dans les deux groupes de traitement sans différence significative (Fig. 2).
Figure 2 – Évolution de l’HbA1c à 3 et 6 mois dans les deux groupes de traitement.
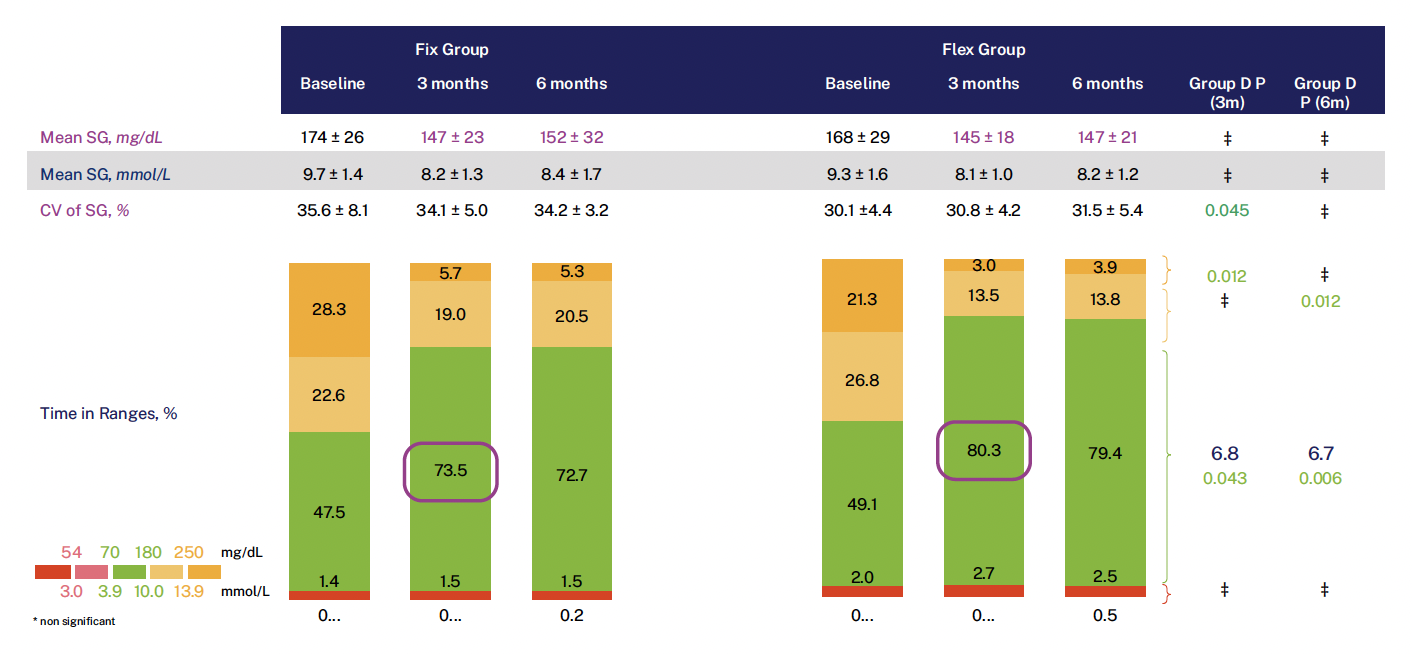
De la même manière, une évolution bénéfique du TIR et du TAR a pu être constatée dans les deux groupes avec cependant une amélioration significativement plus importante dans le groupe comptage précis des glucides à 6 mois (Fig. 3).
Figure 3 – Évolution des paramètres de la mesure continue du glucose à 3 et 6 mois dans les deux groupes de traitement.
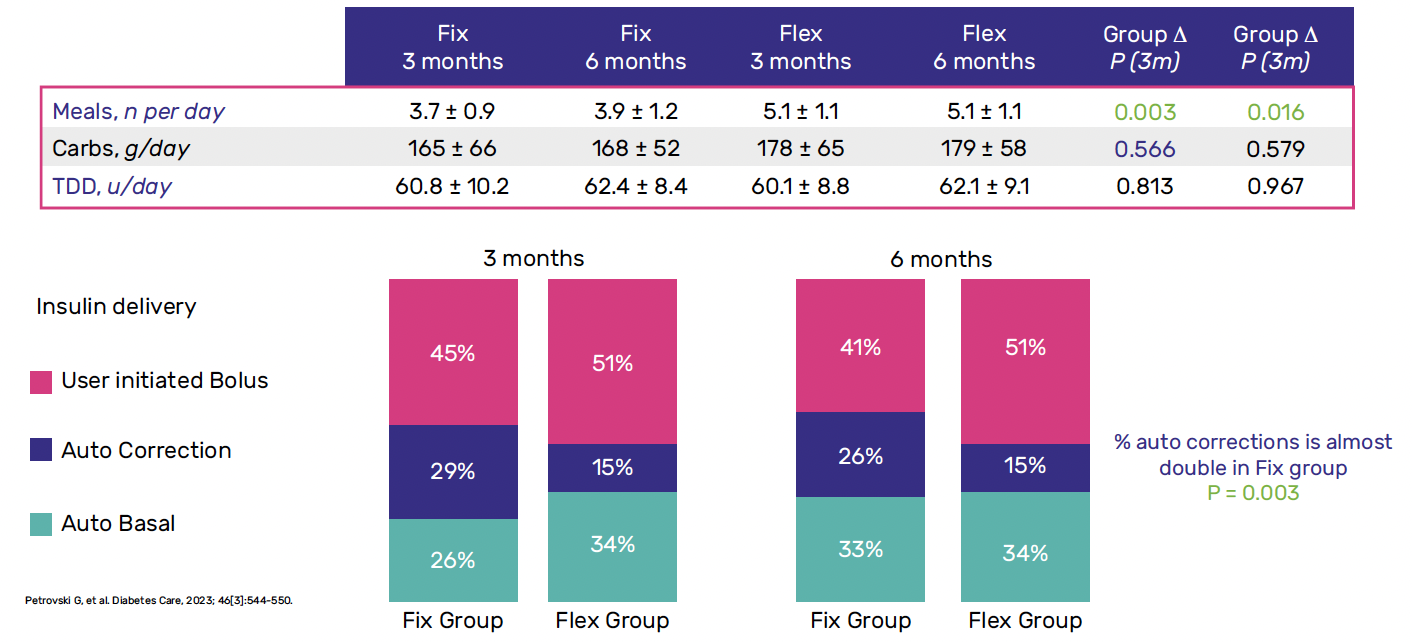
Il est important de noter que ces résultats très bénéfiques obtenus dans le groupe avec annonce fixe des glucides ont été la conséquence d’ajouts de bolus automatiques plus fréquents (26 versus 15 % à 6 mois) que dans le groupe avec comptage précis (Fig. 4).
Figure 4 – Évolution des doses d’insuline à 3 et 6 mois dans les deux groupes de traitement.
À retenir
L’utilisation de quantités individualisées de glucides fixes aux repas chez les patients vivant avec un DT1 traité par boucle fermée permet d’obtenir un temps dans la cible au-delà de 70 % et une HbA1c < 7 % après 6 mois de suivi. Cette approche simplifiée permet de réduire l’effet de la maladie sur la charge mentale des patients grâce à l’adaptation du système automatisé. Une évaluation de cette approche à grande échelle est indispensable désormais pour permettre au plus grand nombre de patients concernés de bénéficier de ces systèmes automatisés de délivrance d’insuline.
• Petrovski G, Campbell H, Pasha M et al. Simplified meal announcement versus precise carbohydrate counting in adolescents with type 1 diabetes using the Minimed 780g advanced hybrid closed loop system: a randomized controlled trial comparing glucose control. Diabetes Care 2023 ; 46 : 544-50.
TOP 4 – Utilité du système flash monitoring glucose dans le diabète de type 2 non traité par insuline, ça se confirme aussi !
L’utilisation de la mesure continue du glucose par système flash glucose monitoring (FGM) est devenue depuis quelques années le standard dans l’autosurveillance des patients vivant avec DT1, mais également dans celle des patients vivant avec un DT2 traité par multi-injections ou pompe à insuline. Rendant possible une adaptation plus précise des doses d’insuline que l’autosurveillance glycémique classique, cet outil permet non seulement d’améliorer la qualité de l’équilibre glycémique au long cours, mais également de réduire les complications aiguës du diabète comme la survenue d’hypoglycémies sévères ou d’acidocétose (1). De plus en plus d’arguments scientifiques viennent positionner le système FGM comme un formidable outil éducatif en dehors de tout traitement par insuline. Au cours du dernier congrès de l’ADA, une très belle session clinique a été consacrée à l’utilisation du FGM chez le patient obèse non diabétique, chez le patient avec pré-diabète et surtout chez le sujet vivant avec un DT2 non traité par insuline.
L’étude IMMEDIATE
C’est ainsi que Ronnie Aronson, diabétologue à Toronto, a présenté les résultats de l’étude IMMEDIATE (2), une étude destinée à évaluer l’intérêt de l’utilisation du FGM comparativement à une autosurveillance glycémique classique chez des sujets vivant avec un DT2. Le design de cet essai projectif randomisé de 16 semaines est reproduit dans la figure 5.
Figure 5 – Schéma de l’étude prospective IMMEDIATE comparant FGM et autosurveillance classique au cours du DT2 non traité par insuline.
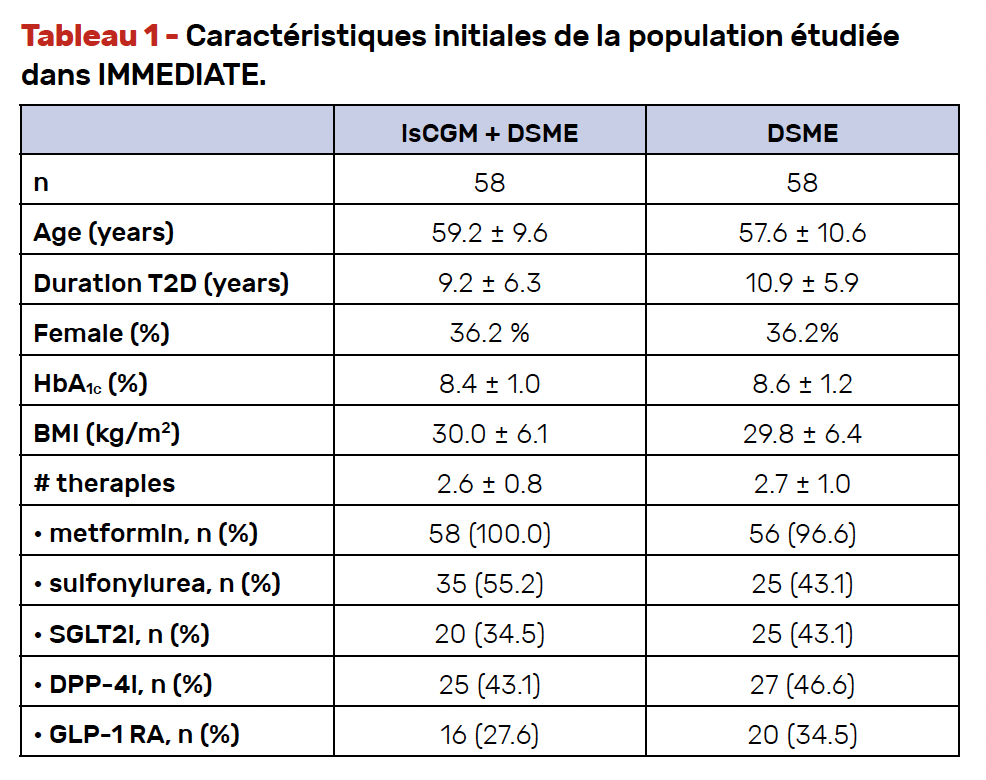
Les caractéristiques des sujets inclus dans cet essai sont reproduites dans le tableau 1. On peut constater qu’il s’agissait de patients ayant une durée d’évolution de la maladie de plus de 9 ans et que leur traitement habituel faisait intervenir plusieurs molécules de modes d’action différents. Il s’agissait donc de sujets ayant une prise en charge thérapeutique (éducative et médicamenteuse) déjà complexe.
Les résultats
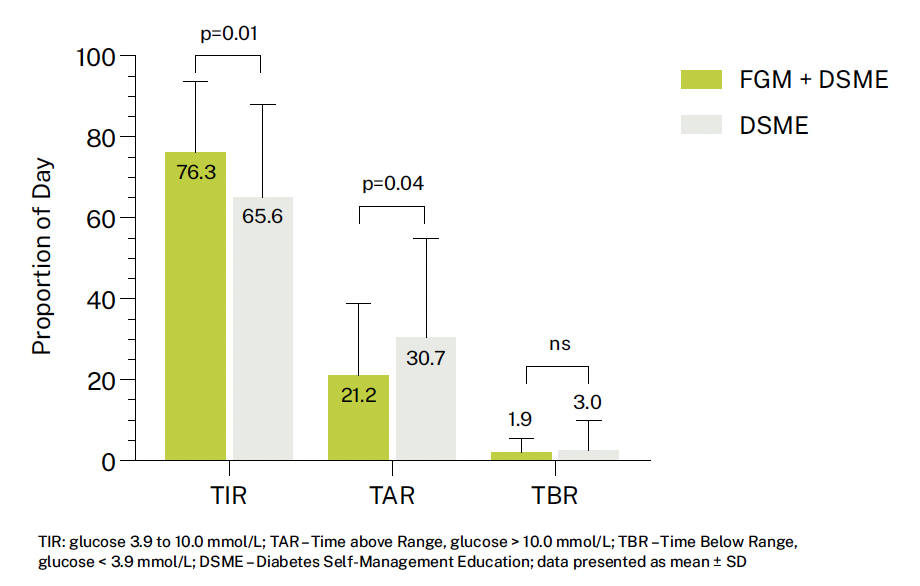
Les résultats de cette étude confirment l’intérêt majeur de l’utilisation du système FGM dans la population de sujets vivant avec un DT2 non traité par insuline avec une amélioration des paramètres TIR, TAR et TBR (Fig. 6) ainsi que de l’HbA1C qui a diminué de façon significative dans le groupe FGM (groupe interventionnel : 7,6 ± 0,9 % (baseline : 8,5 ± 1,0 %) versus groupe témoin : 8,1 ± 1,2 % (baseline : 8,7 ± 1,2 %)). Moyenne des différences ajustées : 0,3 % de moins dans le groupe interventionnel (p = 0,048). Les sujets dans le groupe FGM ont été très satisfaits de l’utilisation de cet outil au vu des résultats des questionnaires analysés.
Figure 6 – Évolution du TIR, du TAR et du TBR dans les deux groupes.
À retenir
L’utilisation du système FGM chez les sujets vivant avec un DT2 s’accompagne d’une amélioration de l’équilibre glycémique avec une excellente tolérance dans cette étude à 16 semaines. D’autres études réalisées chez des sujets dont la maladie évolue depuis peu de temps sont indispensables (en utilisant le système de façon permanente ou intermittente), elles permettront de mieux positionner la place de ce dispositif dans l’évolution du DT2.
1. Roussel R, Riveline JP, Vicaut E et al. Important drop in rate of acute diabetes complications in people with type 1 or type 2 diabetes after initiation of flash glucose monitoring in france: the RELIEF study. Diabetes Care 2021 ; 44 : 1368-76.
2. Aronson R, Brown RE, Chu L et al. Impact of flash glucose monitoring in people with type 2 diabetes inadequately controlled with non-insulin antihyperglycaemic therapy (IMMEDIATE): A randomized controlled trial. Diabetes Obes Metab 2023 ; 25 : 1024-31.
TOP 3 – Association iSGLT2-AR-GLP-1 au cours du diabète de type 2 et risque cardio-rénal : les résultats de vie réelle confirment l’intérêt présumé
La prise en charge thérapeutique du DT2 a évolué ces dernières années d’une approche glucocentrée vers une approche de protection cardio-rénale du fait des effets protecteurs d’organes démontrée avec les iSGLT2 et les AR-GLP-1. Ces deux classes de traitement sont d’ailleurs largement préconisées dans les recommandations de l’ADA et de l’EASD, y compris en association, lorsque les sujets présentent une maladie cardiovasculaire avérée et/ou une atteinte rénale (1).
Cependant, malgré l’intérêt théorique d’une telle association au vu des modes d’action complémentaires et des résultats métaboliques positifs constatés dans les RCT et les études d’observation, nous ne disposons pas actuellement de résultats d’essais prospectifs randomisés (l’essai PRECIDENTD est encore en cours) concernant les effets cardio-rénaux d’une telle association.
L’étude de vie réelle
Lors d’une session particulièrement intéressante consacrée à l’utilisation de ces deux classes de traitement, Sally Lu de Montréal a présenté les résultats d’une étude de vie réelle concernant cette association thérapeutique chez des sujets vivant avec un DT2. Réalisé à partir de trois bases de données épidémiologiques (soins primaires, hospitalisation, registre de décès), ce travail a pris en compte de multiples variables (démographiques, médicales, biologiques, thérapeutiques…) afin de réduire les biais d’interprétation grâce à l’utilisation d’un score de propension optimisé. Deux co-événements ont été retenus comme critère primaire de jugement : le MACE en 3 points et les événements rénaux sérieux (hospitalisations, insuffisance rénale sévère).
Deux cohortes ont ainsi été individualisées :
• la cohorte 1 comparant les sujets utilisant un AR-GLP-1 seul à des sujets utilisant l’association iSGLT2-AR-GLP-1
• et la cohorte 2 comparant les sujets utilisant un iSGLT2 seul à cette même association.
Les résultats
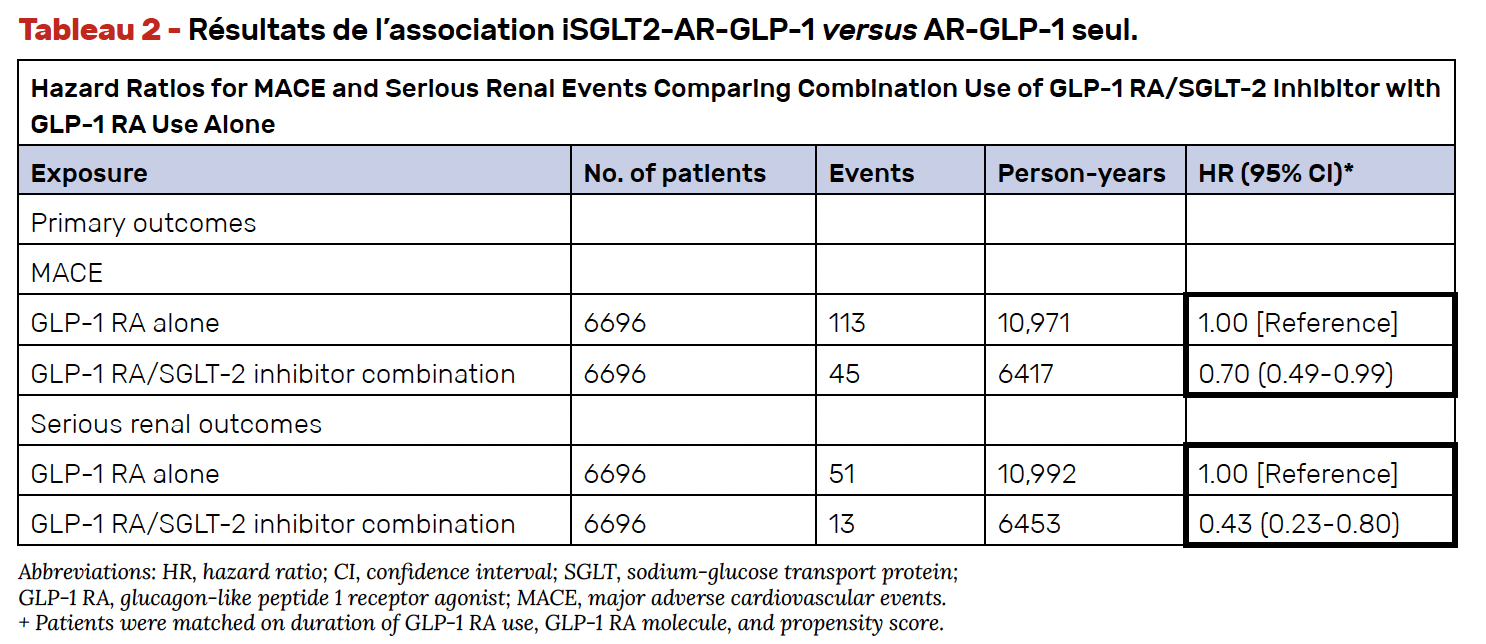
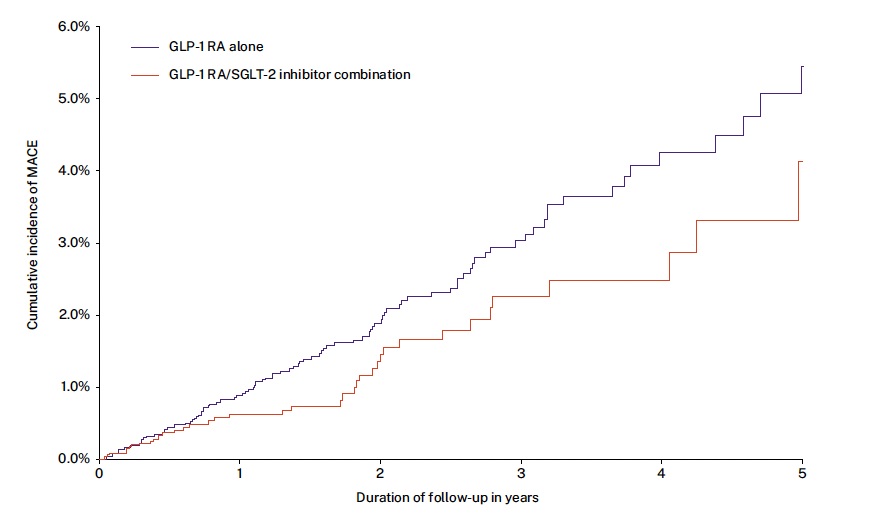
• Les résultats de la cohorte 1 sont représentés dans le tableau 2 montrant une diminution du HR de 30 % pour le MACE et de 57 % pour les événements rénaux sérieux chez les sujets utilisant l’association versus AR-GLP-1 seul. La représentation graphique de ces résultats au cours du temps (Fig. 7) confirme la diminution progressive des événements cardiovasculaires, plus marquée avec l’association iSGLT2-AR-GLP-1.
Figure 7 – Évolution du MACE dans la population traitée par AR-GLP-1 seul versus association iSGLT2-AR-GLP-1.
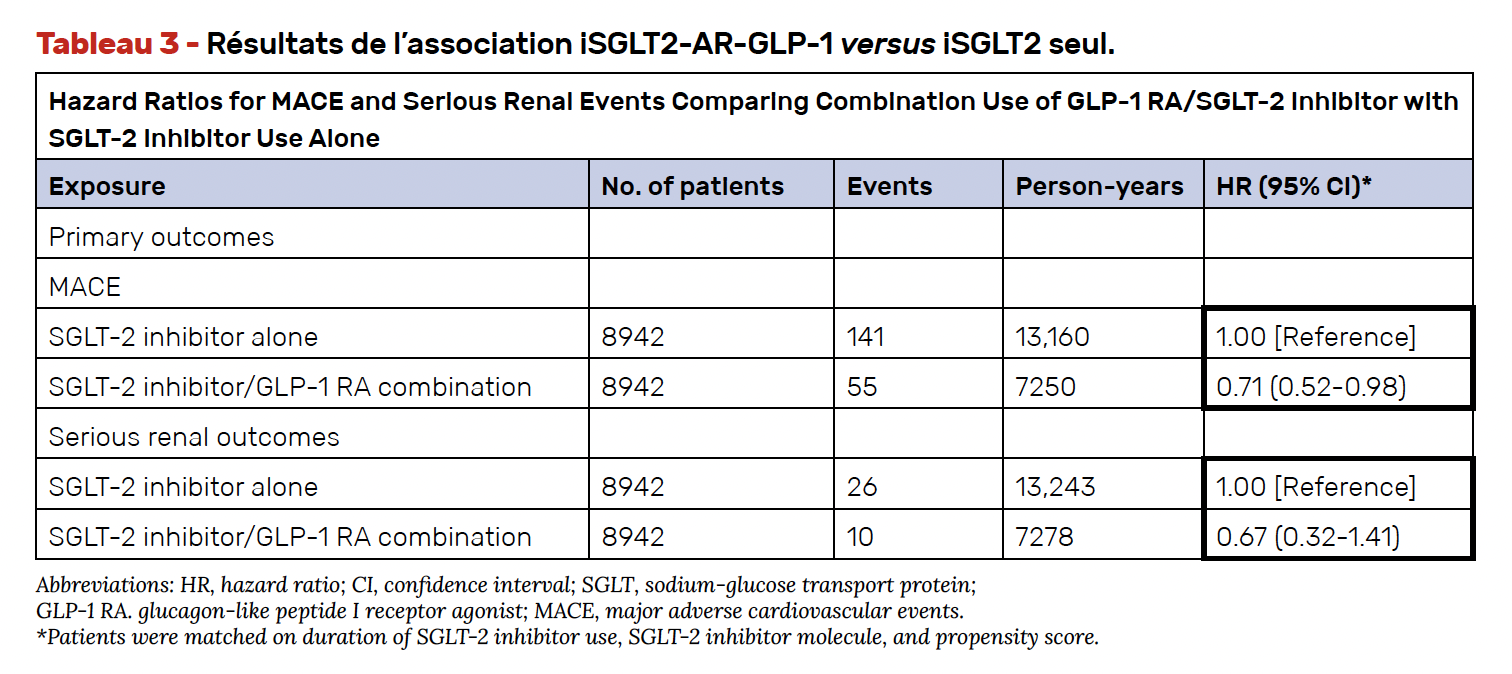
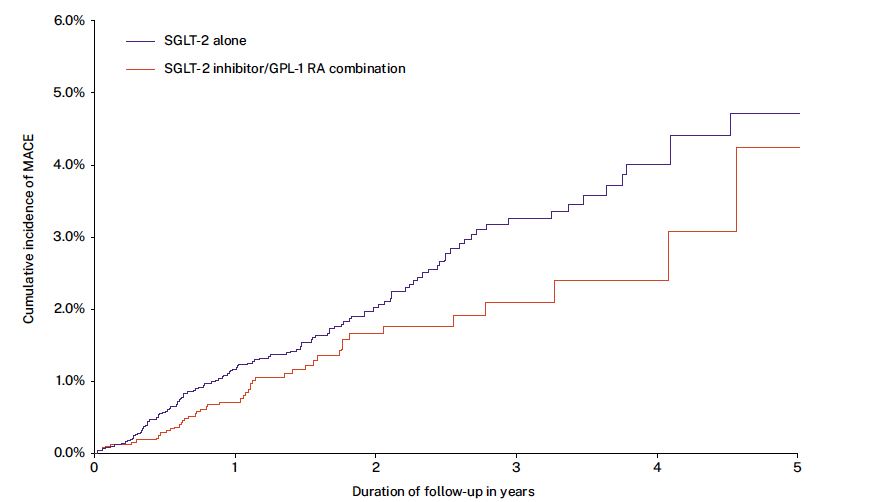
• De la même manière, les résultats de la cohorte 2 sont représentés dans le tableau 3 montrant également un bénéfice de l’association iSGLT2-AR-GLP-1 versus ISGLT2 seul avec une diminution du HR de 29 % pour le MACE 3P et de 33 % pour les événements rénaux sérieux (sans atteindre cependant la significativité). La représentation graphique des résultats de la cohorte 2 au cours du temps (Fig. 8) confirme la diminution progressive des événements cardiovasculaires, plus marquée avec l’association iSGLT2-AR-GLP-1 qu’avec l’utilisation d’un iSGLT2 seul.
Figure 8 – Évolution du MACE dans la population traitée par iSGLT2 seul versus association iSGLT2-AR-GLP-1.
À retenir
Dans cette étude de vie réelle, l’effet protecteur cardio-rénal chez les sujets vivant avec un DT2 est plus marqué avec l’association iSGLT2-AR-GLP-1 qu’avec l’utilisation d’un AR-GLP-1 seul ou d’un iSGLT2 seul. Ces résultats doivent nous conforter dans l’utilisation plus fréquente de cette association thérapeutique.
• Gourdy P, Darmon P, Dievart F et al. Combining glucagon‑like peptide‑1 receptor agonists (GLP‑1RAs) and sodium‑glucose cotransporter‑2 inhibitors (SGLT2is) in patients with type 2 diabetes mellitus (T2DM). Cardiovasc Diabetol 2023 ; 22 : 79.
TOP 2 – Les insulines hebdomadaires arrivent, et ça promet…
Une administration hebdomadaire d’insuline basale au lieu d’une administration quotidienne pourrait permettre d’augmenter l’adhésion des patients, mais également d’améliorer leur qualité de vie, à condition que le risque d’hypoglycémie reste faible (1). Plusieurs approches technologiques ont été proposées afin de ralentir l’absorption ou de prolonger l’action des insulines basales.
Les programmes de développement
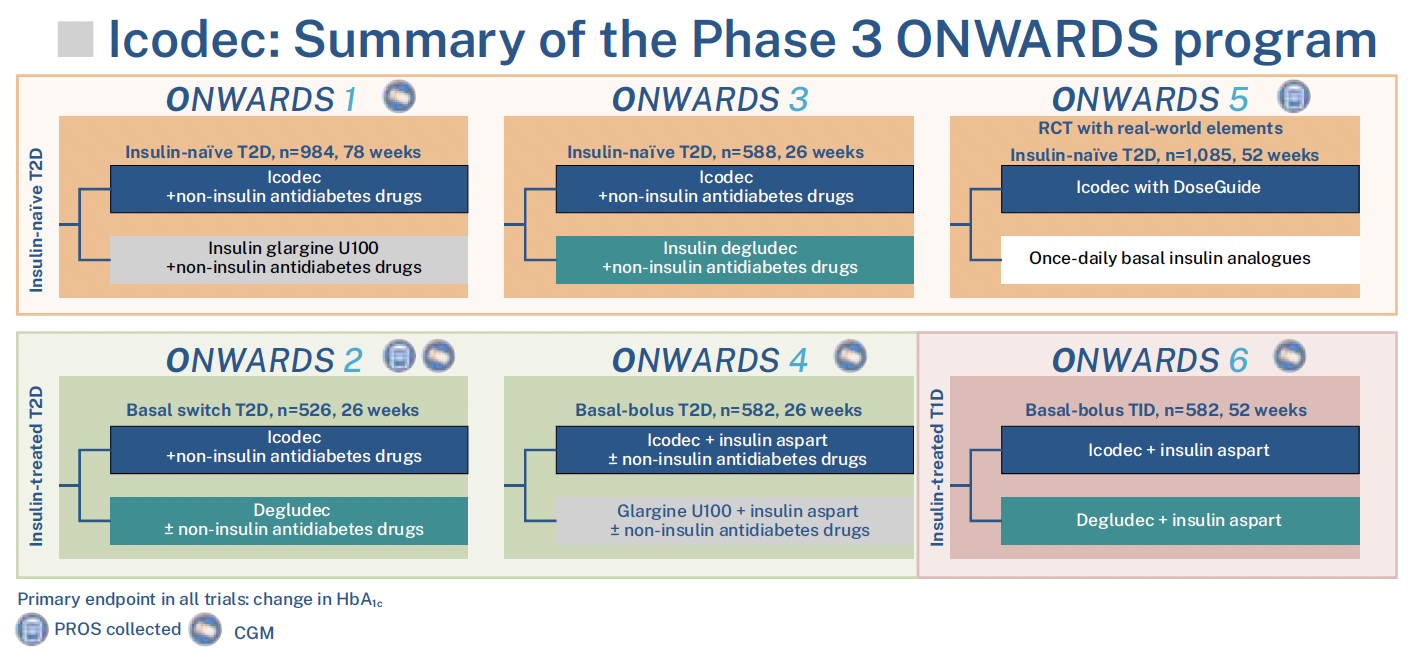
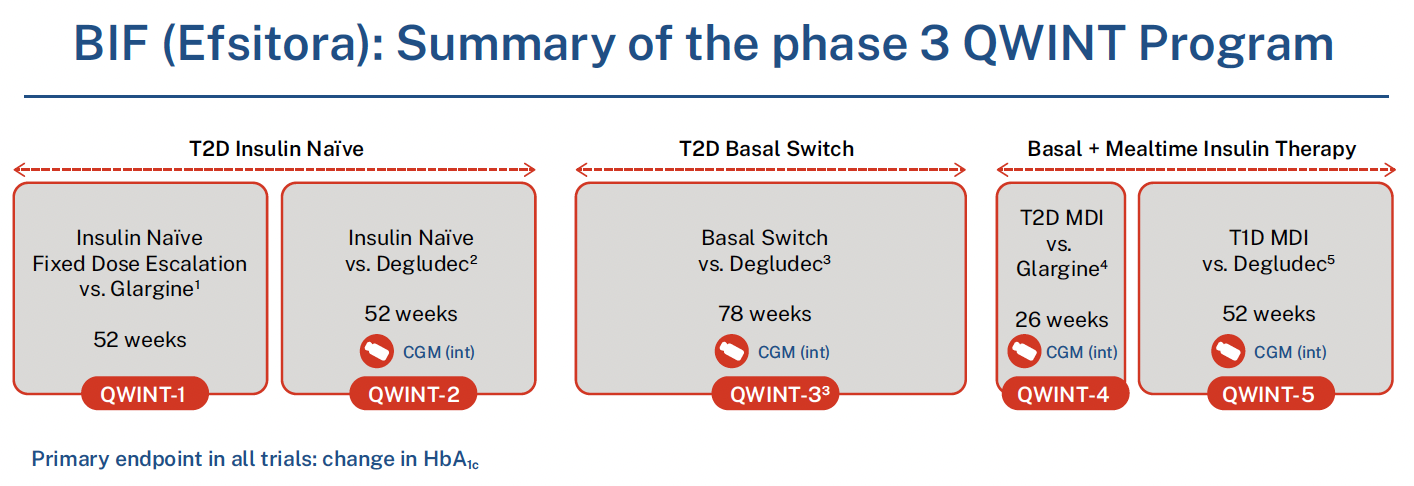
Au dernier congrès de l’ADA une session passionnante a été consacrée au développement de l’insuline icodec (une molécule d’insuline à laquelle un acide gras, l’acide eicosadinoïque, a été fixé à la chaîne B) et de l’insuline efsitora (fixation du fragment FC cristallisable de l’immunoglobuline sur la chaîne B de l’insuline). Le programme de développement clinique de ces deux insulines hebdomadaires a été présenté par Ildiko Lingvay de Dallas qui a détaillé les études cliniques en cours, principalement au cours du DT2, mais également au cours du DT1. Dans la figure 9 est représenté le programme de développement de l’insuline icodec et dans la figure 10 celui d’efsitora.
Figure 9 – Programme de développement de phase III d’icodec.
Figure 10 – Programme de développement de phase III d’efsitora.
Les résultats
Les résultats des études de phase II et de certaines études de phase III ont permis de confirmer l’efficacité et la sécurité d’utilisation de ces insulines hebdomadaires et de préciser la dose hebdomadaire préconisée en initiation (sept fois la dose quotidienne envisagée avec une insuline basale quotidienne) ou en switch d’une insuline basale quotidienne (sept fois la dose quotidienne + une dose de charge équivalente à 50 % de la dose calculée). Le résumé des résultats obtenus dans ces études cliniques est reproduit dans la figure 11.
Figure 11 – Résumé des résultats obtenus au cours des études de phase II et de certaines études de phase III avec les insulines hebdomadaires.
Si le risque hypoglycémique semble finalement le même qu’avec les insulines basales quotidiennes dans le DT2, il reste cependant à mieux préciser chez les sujets vivant avec un DT1 dont la variabilité glycémique est plus importante.
De nombreuses questions restent encore sans réponse à ce jour et la liste non exhaustive de ces questions est reproduite dans la figure 12.
Figure 12 – Liste non exhaustive des questions encore sans réponse concernant les insulines hebdomadaires.
À retenir
L’utilisation des insulines hebdomadaires au cours du DT2 semble de plus en plus envisageable à court terme, seules ou combinées à un AR-GLP-1 hebdomadaire (2). Ces insulines doivent encore faire l’objet d’études spécifiquement dédiées au DT1 et dans certaines situations cliniques particulières.
1. Rosenstock J, Bajaj HS, Janez A et al. Once-weekly insulin for type 2 diabetes without previous insulin treatment. N Engl J Med 2020 ; 383 : 2107-16.
2. Meyer L, Kessler L. Insulines basales hebdomadaires : déjà une réalité ? Correspondances en Métabolismes Hormones Diabètes et Nutrition 2022 ; XXVI : 2.
TOP 1 – Téplizumab et prévention du diabète de type 1, l’espoir
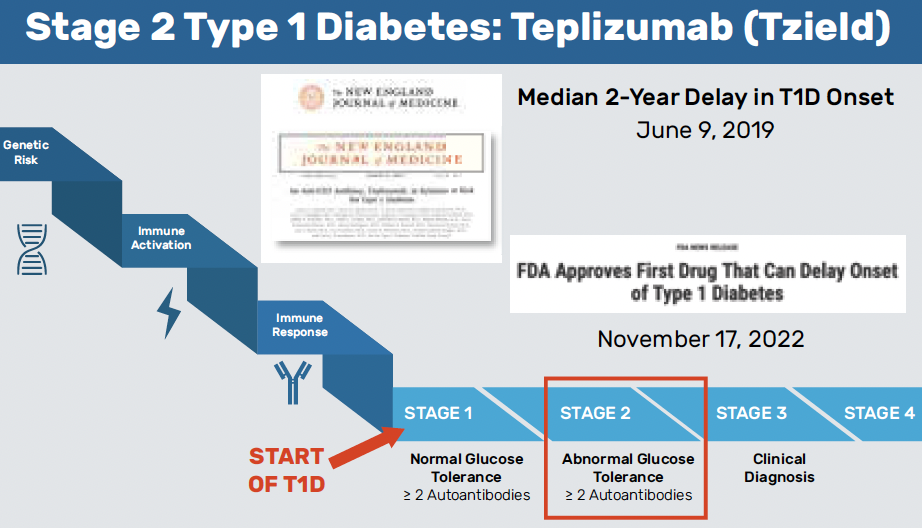
Chez les sujets génétiquement prédisposés, le DT1 se développe progressivement à travers des étapes totalement aymptomatiques avant qu’une hyperglycémie franche se déclare. Ces étapes sont caractérisées par la présence d’auto-anticorps sans dysglycémie (stade 1) puis avec dysglycémie (stade 2) sous la forme d’anomalies post-charge en glucose, mais avec HbA1C normale. Ces différents stades évolutifs permettent d’identifier les sujets à risque de développer un DT1 avec hyperglycémie franche.
Place du téplizumab dans l’évolution naturelle du DT1
Au cours du dernier congrès de l’ADA, une session captivante de bout en bout a été consacrée à l’utilisation de téplizumab, un anticorps monoclonal anti-CD3 dont la FDA a approuvé l’utilisation au cours du stade 2 le 17 novembre 2022.
Helen Leschek du NIH est revenue sur l’évolution naturelle du DT1 et la place du téplizumab dans cette évolution (Fig. 13).
Figure 13 – Évolution naturelle du DT1 et place du téplizumab.
L’utilisation de téplizumab se heurte cependant à un certain nombre d’obstacles au premier rang desquels se trouve le challenge de l’identification des sujets vivant avec un DT1 au stade 2 (Fig. 14).
Figure 14 – Obstacles liés à l’utilisation du téplizumab.
Les résultats
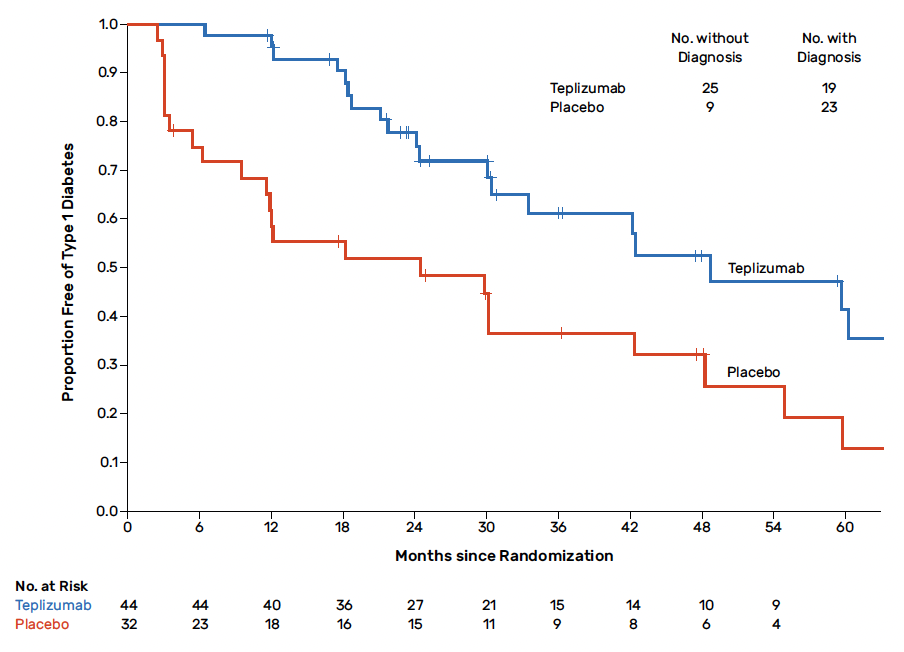
Kevan Herold, de l’université de Yale est revenu sur les résultats de l’étude de phase II réalisée chez 76 sujets à haut risque de développer un DT1 objectivant l’effet bénéfique du téplizumab sur l’apparition d’une hyperglycémie franche (Fig. 15). La durée médiane d’apparition d’un DT1 clinique a été de 48,4 mois dans le groupe téplizumab et de 24,4 mois dans le groupe placebo. Le DT1 clinique a été constaté chez 19 (43 %) des sujets recevant téplizumab et chez 23 (72 %) de ceux recevant le placebo.
Figure 15 – Représentation graphique des résultats du téplizumab chez des sujets à haut risque de développer un DT1 clinique.
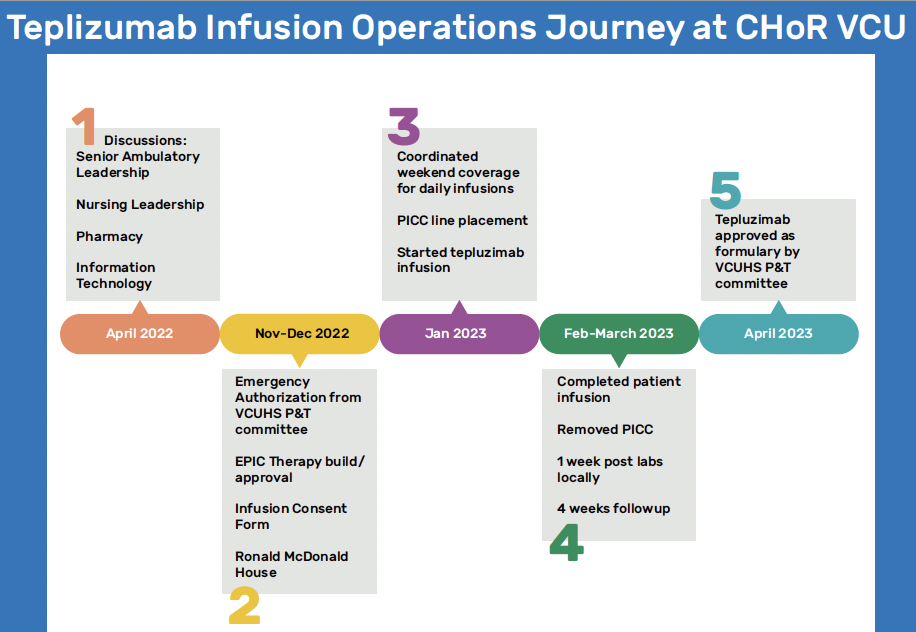
Enfin, Bryce Nelson, de l’université de Richmond, a présenté son expérience de terrain du téplizumab en décrivant le parcours de soins des patients concernés (Fig. 16).
Figure 16 – Parcours de soins de sujets traités par téplizumab à Richmond.
À retenir
Le téplizumab est un formidable espoir dans la prévention du DT1 clinique chez les sujets à haut risque. Il ouvre la voie à de plus en plus de travaux de recherche dans le domaine du dépistage des sujets à risque de diabète de type 1 et de l’immunothérapie préventive.
• Herold KC, , Bundy BN, Long SA et al. An anti-CD3 antibody, teplizumab, in relatives at risk for type 1 diabetes. N Engl J Med 2019 ; 381 : 603-13.
L’auteur déclare ne pas avoir de liens d’intérêt en rapport avec cet article.
Les TOPS 4 ADA 2023 en obésité
Pr Ariane Sultan
TOP 1 – Une révolution dans la prise en charge des personnes en situation d’obésité
Le sémaglutide a révolutionné la prise en charge des personnes en situation d’obésité, par son efficacité sur le poids, mais également par la tant attendue reconnaissance de l’obésité en tant que pathologie chronique. Il ne sera malheureusement plus disponible en initiation de traitement, mais pourra continuer d’être utilisé dans le cadre d’un renouvellement de traitement.
Le tirzépatide
Le tirzépatide est à la fois un agoniste du récepteur au GLP-1, et également un agoniste du GIP (Glucose-dependent Insulinotropic Polypeptide). Le GIP possède notamment une double fonction : glucagonotrope en cas de normoglycémie et d’hypoglycémie, et glucagonostatique en cas d’hyperglycémie. La perte de poids induite par les agonistes du récepteur GIP est donc due principalement à l’effet anorexigène et anti-lipogènique du glucagon.
L’étude SURMOUNT-2
L’étude SURMOUNT-2, étude randomisée contrôlée en double aveugle, a été présentée dans le cadre d’un symposium à l’ADA et publiée le même jour dans The New England Journal of Medicine. L’objectif de l’étude était d’évaluer l’intérêt d’un traitement par tirzépatide 10 et 15 mg (avec une période d’escalade de dose) versus placebo chez des sujets en situation de surpoids (IMC supérieur à 27 kg/m², IMC moyen = 36 kg/m²) et un diabète de type 2 (HbA1c moyenne = 8 %, durée d’évolution moyenne du diabète = 8,5 ans).
Les résultats
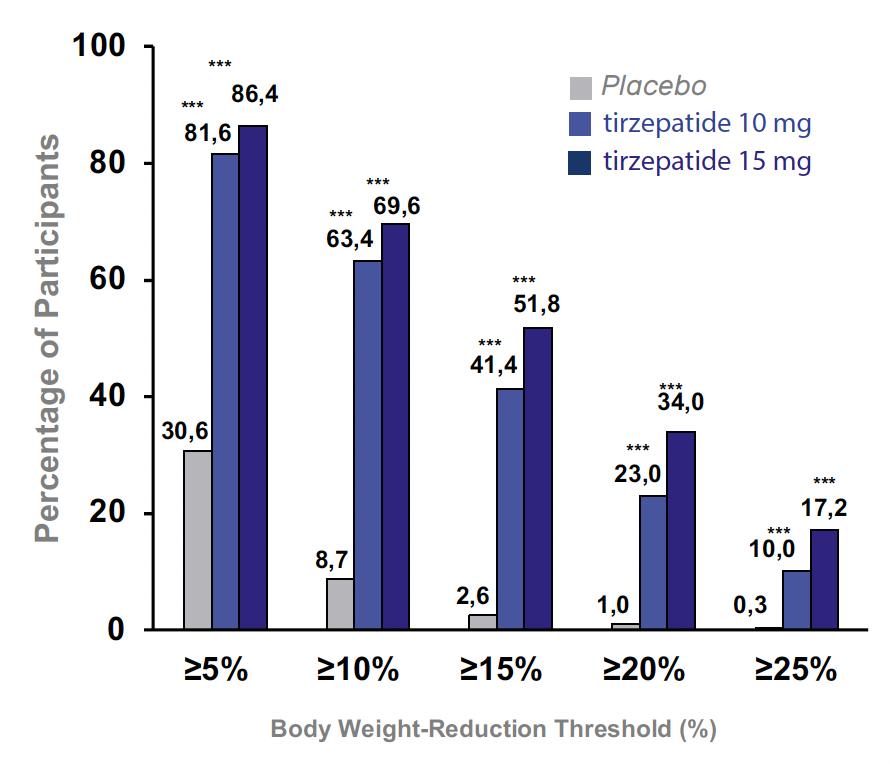
À 72 semaines, le traitement était associé à un pourcentage de perte de poids de 12,8 et 14,7 % respectivement sous tirzépatide 10 et 15 mg versus 3,2 % sous placebo. 63,4 % des sujets sous tirzépatide 10 mg et 69,5 % des sujets sous tirzépatide 15 mg ont perdu plus de 10 % de leur poids corporel. 23 % des sujets sous tirzépatide 10 mg et 34 % des sujets sous tirzépatide 15 mg ont perdu plus de 20 % de leur poids corporel (Fig. 1). À 72 semaines, le traitement était associé à une baisse de l’HbA1c de 2 % sous tirzépatide 10 et 15 mg versus 0,5 % dans le groupe placebo. Plus de 80 % des sujets atteignent la cible d’HbA1c inférieure à 7 %. Le pourcentage d’effets secondaires était comparable entre les trois groupes.
Figure 1 – Pourcentage de perte de poids sous tirzépatide versus placebo.
À retenir
Ces résultats viennent confirmer ceux très positifs de SURMOUNT-1, qui avait inclus des sujets avec un IMC ≥ 30 kg/m² ou ≥ 27 kg/m² avec une complication liée au poids. Cette étude avait montré que le traitement était associé à un pourcentage de perte de poids de 19,5 et 20,9 % respectivement sous tirzépatide 10 mg et 20 mg versus 3,1 % sous placebo. Ces résultats sont donc extrêmement encourageants. À quand la molécule en France ?
TOP 2 – La chirurgie métabolique : des données en fonction de l’IMC
Le terme “chirurgie métabolique” correspond au traitement chirurgical du diabète de type 2 (DT2), c’est-à-dire ayant pour objectif principal la rémission du diabète. Les méta-analyses démontrent un bénéfice significatif de la chirurgie métabolique (sleeve gastrectomy, by-pass gastrique…) versus une prise en charge médicale en termes de taux de rémission du DT2 à 24 et 36 mois dans l’obésité de grade 1, 2 ou 3 (cinq études randomisées). Aucune étude randomisée dédiée aux personnes en situation d’obésité de grade 1 n’a cependant été réalisée, seule l’analyse en sous-groupes des cinq études citées plus haut, qui concerne seulement 80 personnes, permet à ce jour de supposer un bénéfice chez ces sujets. Il est donc essentiel d’obtenir plus de données.
L’étude ARMMS-T2D
L’étude ARMMS-T2D a analysé les résultats de quatre études randomisées (chirurgie métabolique versus traitement médical) de façon à obtenir des résultats statistiquement plus puissants que ceux obtenus avec une étude unique.
À retenir
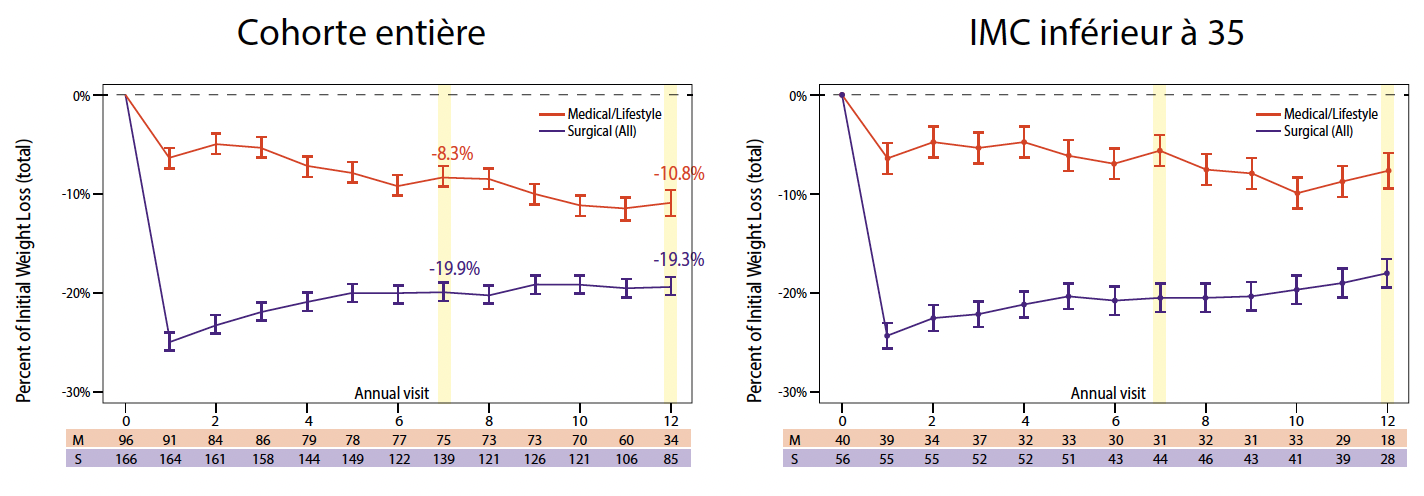
Les résultats montrent que le pourcentage de perte de poids obtenu avec la chirurgie est comparable entre le sous-groupe de sujets avec IMC inférieur à 35 et la cohorte entière (Fig. 2).
Figure 2 – Pourcentage de perte de poids chirurgie versus traitement médical en fonction de l’IMC.
TOP 3 – L’application des recommandations en pratique clinique : un défi !
On le sait, la mise en place des recommandations en pratique clinique est difficile, et prend un certain délai…
L’étude COORDINATE-Diabetes
L’étude COORDINATE-Diabetes a évalué l’effet d’un programme global incluant formation, parcours de soins et coordination des soins versus prise en charge selon les habitudes des équipes, dans des centres de cardiologie américains, sur le taux de prescription des trois classes thérapeutiques recommandées (statine forte intensité, bloqueurs du système rénine angiotensine, iSGLT2 ou analogue du R-GLP-1) dans la prise en charge des personnes vivant avec un DT2 et antécédents cardiovasculaires.
À retenir
La mise en place de ce programme a ainsi permis une augmentation des taux de prescription de ces trois classes thérapeutiques, de 14 à 37,9 %, ce qui est significativement différent… même si l’on peut quand même considérer que ce résultat est loin d’être parfait…
TOP 4 – Triple agonisme GLP-1, GIP, glucagon dans la prise en charge des personnes vivant avec un diabète de type 2
L’arrivée des triples agonistes va certainement révolutionner la prise en charge des personnes vivant avec un DT2.
L’étude
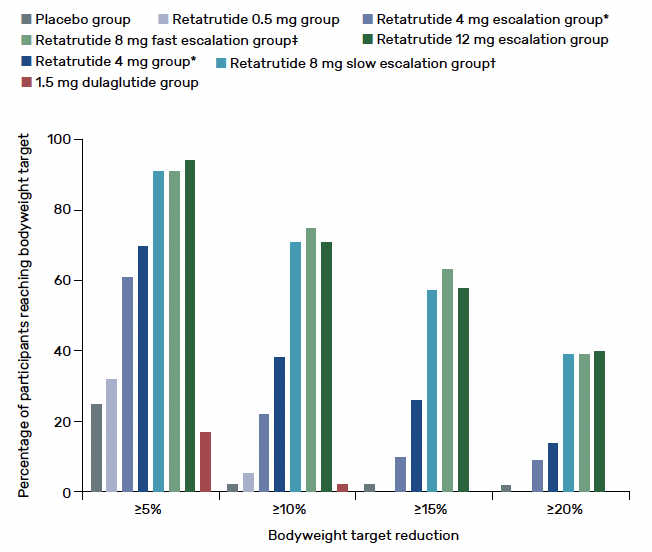
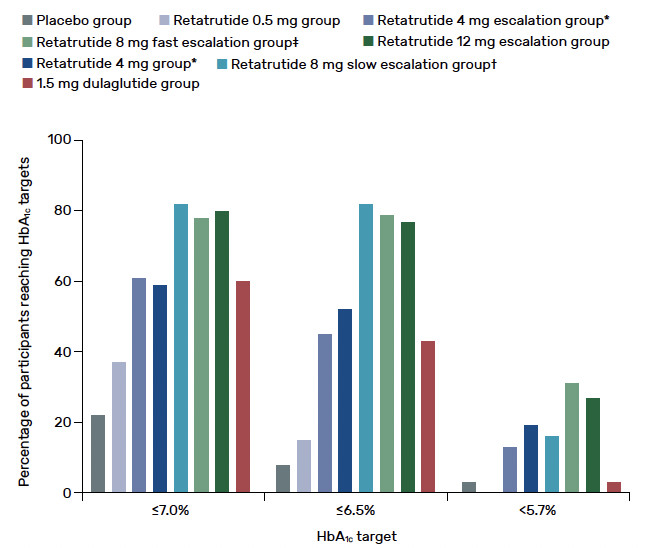
Présentée à l’ADA, cette étude de phase II, randomisée avec rétatrutide à différentes posologies versus dulaglutide 1,5 mg versus placebo apporte des résultats très encourageants en termes de perte de poids et de baisse de l’HbA1c, nettement supérieurs à ceux obtenus sous dulaglutide (Fig. 3 et 4). Étaient inclus des sujets présentant un DT2 (HbA1c moyenne = 8,3 %, IMC moyen = 35 kg/m2).
Figure 3 – Pourcentage de perte de poids, rétatrutide versus placebo versus dulaglutide.
Figure 4 – Pourcentage de sujets à la cible d’HbA1c, rétatrutide versus placebo versus dulaglutide.
À retenir
Les bénéfices pondéraux confirment ceux obtenus spécifiquement chez des sujets en situation d’obésité. On attend désormais les études de phase III.
L’auteur déclare avoir des liens d’intérêt avec Lilly.
L’ADA 2023 en bref
Dr Bernadette Dijoux
À l’ADA 2023, de nombreuses communications présentaient les réflexions des experts, au sortir des études, sur des traitements existants, futurs et à venir. Les différentes équipes ont à cœur de trouver des molécules qui traitent le diabète et l’obésité plutôt que de simplement normaliser une glycémie et/ou perdre du poids.
Les traitements médicamenteux
Le risque cardiovasculaire
Les iSGLT2 et les analogues du GLP-1 continuent de prouver leur efficacité chez les diabétiques et les patients à haut risque cardiovasculaire. Ces molécules ont eu une incidence sur les recommandations pour agir sur le risque cardiovasculaire indépendamment de la glycémie. Selon le Pr MacGire (université du Texas), il faut les utiliser en première intention quelle que soit la glycémie.
Depuis la parution de l’étude EMPAREG, il y a clairement un changement de paradigme pour les cardiologues. Pour le Pr Taub, qui a confirmé l’efficacité de ces traitements, le DT2 et les maladies cardiovasculaires, l’athéro-sclérose sont sous-tendus par les mêmes mécanismes, à savoir : la dyslipidémie, l’inflammation, l’hypercoagulabilité, la dysfonction endothéliale.
Les études vont s’élargir sur l’effet de ces molécules sur la NASH, la NAFLD, la maladie d’Alzheimer, les AVC, le SAOS et la fibrillation atriale.
Le Dr Carlos Santos, cardiologue, étudie particulièrement les mécanismes d’action des iSGLT2 dans l’insuffisance cardiaque quelle que soit la FEVG. La sotaglifozine, qui associe SGLT1 et T2, a notamment été acceptée en mai dernier par la FDA pour les patients cardiaques quelle que soit la FEVG.
Les analogues des incrétines
Le sémaglutide
Les analogues du GLP-1 ont été les premières molécules utilisées. Le sémaglutide a été accepté en 2005 par voie injectable uniquement. Ce qui, comme l’a souligné le Pr Philippe Knop, a gêné sa prescription en première intention. Il existe maintenant sous forme orale.
Les études OASIS-1, avec la dose de 50 mg, et Pionners confirment les études antérieures sur la baisse de HbA1C, du poids, de la glycémie à jeun, le changement de profil lipidique et la baisse de la TAS et TAD.
Les récepteurs du GLP-1 ont donc été la première cible. D’autres traitements se sont développés, combinant et ciblant plusieurs récepteurs simultanément.
Le tirzépatide
Le tirzépatide associe GIP et GLP-1. Selon le Pr Campbell (université Duke), il agirait surtout par l’action sur le récepteur GIP. En effet, chez les souris R-GIP KO, il n’y a pas de baisse de la glycémie, ni chez les souris R-GLP-1 KO. En revanche, dans les cellules d’îlots, si l’on bloque R-GIP, on anéantit l’effet du tirzépatide. Il ne serait donc pas un super-agoniste du GLP-1, mais serait un agoniste multirécepteur qui agit surtout sur le R-GIP.
Le rétatrutide
Le rétatrutide associe trois analogues, R-GIP, R-GLP-1 et glucagon. La nouveauté réside donc dans la présence du glucagon pour baisser la glycémie. Le Pr Sainayl (Virginie) s’est attardé sur l’efficacité de la molécule dans la NFALD et la NASH. Il a rappelé que 5 à 7 % des DT2 développent une NASH. GIP et GLP-1 ont une action sur l’appétit et le diabète, ils agissent sur la NASH de façon indirecte et n’ont pas d’effets directs sur la fibrose hépatique. Il a précisé qu’il n’y a pas de R-GIP ni de R-GLP-1 dans le foie et donc que l’action du traitement serait liée à la présence de glucagon. Le rétatrutide pourrait selon lui être le premier traitement du diabète permettant, grâce au glucagon, d’améliorer directement la maladie hépatique, l’ajout du glucagon aiderait peut-être à gérer de façon holistique les multiples morbidités liées au diabète. Il apporte un effet anti-fibrosique et améliore le profil biliaire, ce qui réduit également la fibrose.
Le Pr Sainayl étudie le sous-groupe NAFLD dans une étude de phase II avec une injection par semaine de rétatrutide à la dose de 8 à 12 mg. Les résultats montrent que 80 % des patients ont une réduction moyenne de la graisse hépatique de 70 à plus de 80 %. La stéatose hépatique disparaît dans 85 % des cas à 48 semaines. À 12 mg, 90 % des patients normalisent la graisse hépatique.
Pour le Pr David Alexis, le glucagon et l’insuline ont longtemps été vus comme un couple antagoniste. Cependant, l’action du glucagon n’est pas gluco-centrée, mais comporte d’autres mécanismes utiles au traitement du diabète dont le plus intéressant est la baisse de la graisse hépatique, avec baisse des triglycérides et des acides gras.
L’amyline et ses analogues
Le Pr David Lau (Calgary, Alberta, Canada) a rappelé que l’obésité était une pathologie chronique qui conduit à des complications qui sont améliorées par la perte de poids. Il a fait le point sur l’amyline, un peptide neuro-endocrine dont l’une des fonctions majeures est la suppression de la libération du glucagon et l’inhibition de la prise alimentaire. Les analogues de l’amyline de longue durée d’action entraînent une diminution du poids par action centrale de l’appétit et se développent pour traiter obésité et diabète. Par exemple, le cagrilintide qui régule l’appétit en agissant sur différentes régions du cerveau est en étude de phase II. Par ailleurs, le premier analogue de l’amyline, le pramalintide, est utilisé en adjonction de l’insuline dans le DT1 et DT2 pour perdre du poids. De plus, l’association cagrilintide-sémaglutide, le CagriSéma, fait l’objet d’une étude de phase II, multicentrique en double aveugle sur 32 semaines versus sémaglutide seul et cagrilintide seul. L’association aurait peu d’effets sur la glycémie, mais entraîne des pertes de poids de 20 à 30 % comparables à l’effet des chirurgies bariatriques.
Le peptide YY
Le Pr Tricia Tan (Royaume-Uni) a présenté cette molécule connue depuis 1980. Il s’agit d’une autre hormone du tube digestif, existant sous deux formes PYY-1-36 et 3-36 qui ont des effets physiologiques différents. PYY3-36 + GLP-1 ont un effet synergique prouvé par une méthode d’imagerie centrale ; PYY3-36 n’a pas d’effet sur l’insulinosécrétion et GLP-1 conserve son effet sur l’insulinosécrétion. Six traitements sont en cours d’étude, le plus souvent en association.
Le PYY-1-36 est également à l’étude…
À retenir
Le Pr Jastreboff (université de Yale) considère que la découverte de l’insuline avait été un moment crucial en médecine et que, actuellement, l’introduction de ces traitements anti-obésité crée un nouveau tournant. « Nous nous plaçons dans une position qui permettra de traiter une pathologie qui potentiellement cause ou contribue à 200 autres pathologies liées au poids. » Cependant, « Ces molécules induisent des pertes de poids considérables, ce qui est une partie de la solution. L’objectif doit être de traiter l’obésité et de cibler la physiopathologie neuro-métabolique de l’obésité et les différents mécanismes en cause, car il existe plusieurs types d’obésités. »
La diététique reste présente
La diète transitoire à 800 calories
Le Pr Roy Taylor est convaincu de l’effet bénéfique d’une diète transitoire à 800 calories, car, dans le DT2, le plus important est la perte de poids. Dans l’étude DIRECT, il constate en 7 jours une baisse de 30 % de la graisse hépatique, une augmentation progressive de la fonction cellulaire bêta en 8 semaines. Le pourcentage de graisse hépatique passe de 36 à 2 % et se maintient à 6 mois.
Les régimes LCD et VLCD
Le Pr Nia Schwann Mitchell a fait le point sur les régimes LCD (low-calorie diet) et VLCD (very low-calorie diet) : l’adhésion à ces régimes induit une baisse de 47 % de l’HbA1C à 6 mois avec stabilité sur 12 à 24 mois ; et une rémission du DT2 de 87 % est observée dans les méta-analyses avec arrêt des médicaments, ainsi qu’une baisse des triglycérides et une augmentation de HDL. Cependant, les patients adhèrent plus à une low fat diet et à un régime méditerranéen qu’aux LCD et VLCD.
Les indices glycémiques bas
Pr Daniel Cox a rappelé que les aliments à indice glycémique bas diminuaient le pic glycémique et accéléraient le retour à la normale, réduisant ainsi la glycémie post-prandiale. Les patients testent leur glycémie et choisissent progressivement les aliments les plus favorables. Cette notion était associée à un changement de mode de vie avec plus d’activité physique modérée, augmentation du temps de sommeil, moins de temps assis. Ce changement de mode de vie permet une baisse de l’HbA1C et de l’IMC, une augmentation de l’autonomie et une amélioration psychique.
Les recherches soutenues par l’ADA
L’ADA soutient les nouvelles recherches dans le diabète, l’objectif étant là aussi de trouver un traitement du diabète.
Le microbiote digestif
Le tube digestif a toujours été reconnu comme un acteur clé du diabète. Le vrai acteur est peut-être le microbiote. Le Pr Kostic (Harvard) développe l’action immuno-régulatrice du microbiote digestif.
• Sur les 150 trillions de microorganismes, nombre d’entre eux aideraient à traiter le diabète en modulant la tolérance immune, en induisant des cellules T régulatrices pour bloquer l’activité immune des T Killers et protéger la cellule bêta et l’insulinosécrétion.
• Les études dans le DT1 comparent le microbiote de sujets finlandais en population urbaine versus milieu rural avec un mode de vie traditionnel. Les mêmes différences se retrouvent dans le microbiote des populations de chasseurs et les athlètes de haut niveau. L’incidence du DT1 est six fois plus haute dans les populations urbaines.
• Dans les études de laboratoire, l’adénosine favorise la tolérance immune, promeut la colonisation du tube digestif et l’homéostasie immune. L’inoculation d’espèces appropriées sur des souris obèses diabétiques sans flore intestinale augmente le signal adénosine induisant une augmentation de la masse cellulaire bêta et l’insulinosécrétion. Sont également observées une amélioration de la thermogenèse et la régulation d’autres processus défectueux dans le DT1.
Protéger la cellule bêta contre l’attaque autoimmune
Remplacer les cellules bêta abîmées ou utiliser des cellules souches peut aider, mais les nouvelles cellules peuvent être attaquées par le système immunitaire. Selon le Pr Judith Agudo (Harvard), certaines cellules bêta échappent à l’attaque auto-immune. Du JEDI (jus EGFP Death Inducing) est utilisé sur les cellules T pour mimer le DT1. On a découvert des niveaux de Goldilocks du système majeur d’histocompatibilité permettant d’échapper aux cellules T et NK. Il s’agit de fabriquer des îlots protégés contre les cellules immunes pour échapper à l’attaque auto-immune.
Les BCAA : Branched Chain Amino Acids
Ces acides aminés contribuent au risque de diabète. En activant leur oxydation, on module l’homéostasie, on diminue la graisse hépatique et on améliore le contrôle du glucose. La chaîne régulatrice est l’alpha-kéto acid, BCKA, qui jouerait aussi un rôle dans la dysfonction cardiaque. La protéine phosphatase 1K, PM1K, est associée à la stéatose hépatique.
L’objectif est d’identifier les facteurs régulés par BCKA et PM1K et d’explorer les potentiels thérapeutiques des modulateurs du rapport BCKA/PM1K.
Les recherches visant l’auto-immunité
Dans le DT1, les recherches visent l’auto-immunité dirigée contre les cellules bêta.
Le téplizumab
En 2022, la FDA a approuvé le téplizumab, anti-CD3, qui, prescrit au stade 2 du diabète chez des sujets susceptibles de devenir diabétiques de type 1, permet d’éviter ou de retarder la progression vers le stade 3. Cependant, plusieurs problèmes semblent se poser pour ce traitement :
• il est prescrit en perfusion sur 14 jours, ce qui nécessite une hospitalisation, qui semble compliquée pour des patients éloignés des centres ;
• il présente des effets secondaires,
• est coûteux,
• et, surtout, qui dépister ?
Pour ces diverses raisons, les recherches se poursuivent sur d’autres molécules et souhaitent agir encore plus précocement, en stade 1 du diabète, pour une meilleure efficacité.
L’abatacept
La molécule abatacept est un modulateur sélectif, co-stimulateur qui bloque l’activation des cellules T par le CD28, sur les cellules présentant l’antigène. Il affecte aussi les T-helper folliculaires et périphériques.
• Dans une étude de phase III, ce produit a prolongé de façon saine et efficace la « Lune de miel ».
• Le Dr Russel a par ailleurs publié une étude de phase II randomisée versus placebo testant l’abatacept pour retarder le DT1 au stade 1 dans de fratries à risque de DT1. Douze mois de traitement ont changé les cellules immunes et amélioré le peptide C.
L’hydroxychloroquine
L’hydroxychloroquine interagit avec l’activité lysosomale, l’autophagie et la stabilité de la membrane, elle altère l’activité de transcription, donc a de nombreux effets qui empêchent la destruction auto-immune de la cellule bêta.
Les autres questions sont :
• qui dépister ?
• comment dépister les patients au stade 2 du diabète ?
• existe-t-il des marqueurs métaboliques ou immunologiques pour identifier les patients pouvant répondre au traitement par téplizumab ou autre ?
La proinsuline et synthèse de l’insuline
Le rapport proinsuline/peptide C
Il semble que le rapport proinsuline/peptide C soit prédictif de l’apparition du DT1 dans l’année qui suit. La proinsuline est un bon marqueur de stress de la cellule bêta chez le prédiabétique et le diabétique. C’est un bon prédicteur du diabète. L’augmentation de la proinsuline précède l’apparition du diabète de 12 mois en moyenne. Si le rapport proinsuline/peptide C est élevé, la réponse au téplizumab est meilleure (étude Trialnet).
SERCA
Le Pr Evans étudie la cellule bêta depuis de nombreuses années et a expliqué que, dans cette cellule, les ions calcium jouent un rôle dans la régulation de la cascade de signaux qui aboutissent à la synthèse de l’insuline.
• La pompe membranaire sarco-endoplasmique R Ca++ATPase (SERCA) mobilise le calcium à travers la cellule pour faciliter la maturation de la proinsuline en insuline.
• L’une des voies de dysfonction de la cellule bêta dans le diabète est la diminution de l’expression de SERCA2 qui induit une diminution de la prohormone convertase, une baisse de la conversion, une accumulation de proinsuline dans le réticulum endoplasmique et le Golgi, une altération du calcium mitochondrial.
• La baisse de SERCA2 induit également des cellules bêta affaiblies et plus immunogéniques avec une augmentation de la production d’anticorps.
• Il pourrait aussi exister une activation immune médiée par la mitochondrie.
D’autres molécules apparaissant lors du stress de la cellule bêta sont à l’étude : PDTA1, NUCB2, P4HB. Le PDTA1 est nécessaire à la maturation d’une proinsuline efficace et serait un biomarqueur utile du DT1.
Agir sur les cellules sénescentes
Les études sur les processus fondamentaux du vieillissement qui sont la cause de pathologies ont montré le rôle de la cellule sénescente dans les maladies endocrines, dont le diabète. Différentes approches sont possibles.
Les drogues sénolytiques
Elles sont étudiées par le Pr James Kirkland. Elles éliminent les cellules sénescentes. Elles améliorent l’insulinorésistance, diminuent l’inflammation du tissu adipeux, préviennent les complications comme la stéatose, la dysfonction rénale, oculaire et cérébrale du diabète.
L’approche immunothérapeutique
L’approche immunothérapeutique est préconisée par le Pr Anil
Busham. En effet, les cellules sénescentes persistent à cause d’une faiblesse du système de surveillance immunitaire qui, en temps normal, les élimine naturellement. En réactivant ce système immunitaire défaillant, les cellules sénescentes seraient éliminées par des voies physiologiques.
All is connected!
Des nouveautés dans les interactions des cellules d’îlots ont aussi été présentées lors de cette édition de l’ADA.
Les différents types de cellules d’îlots
Pour rappel, il existe cinq types de cellules d’îlots :
• Alpha Cell libère du glucagon,
• Beta Cell libère de l’insuline,
• Delta Cell libère de la somatostatine,
• Gamma Cell libère le polypeptide pancréatique,
• Epsilon Cell libère de la ghréline.
Ces cinq types cellulaires inter-agissent de façon essentielle dans l’homéostasie du glucose.
Le Dr Golson travaille sur la relation entre les cellules bêta et delta. Delta est activée par des signaux venant de bêta et, indépendamment de cela, répond à des variations glycémiques. Les delta produisent la somatostatine et sont plus riches en leptine que les bêta. La leptine diminue la synthèse d’insuline par les îlots. Les souris leptine + ont une tolérance au glucose améliorée, dans une alimentation équilibrée.
La somatostatine protégerait la cellule bêta et limite la sécrétion d’insuline pendant le stress.
L’axe foie-cellule alpha
Le Pr Danielle Dean définit un interactome comme la synthèse de toutes les interactions entre les cellules et les organes. Les cellules pancréatiques interagissent avec le tissu adipeux, le muscle squelettique, le cerveau, les intestins et, le plus important, le foie. L’axe foie-cellule alpha régule les inter-actions entre les acides aminés produits par le foie et le glucagon produit par la cellule alpha, car cette cellule capte les acides aminés et induit la sécrétion d’insuline.
En diminuant la sécrétion hépatique de glucose et la glycémie, on altère la clairance des acides aminés dans le foie, ce qui induit une hyper-amino-acidémie. L’augmentation du taux de glutamine et surtout d’arginine stimule la cellule alpha, entraîne une hypersécrétion de glucagon, une prolifération et une hyperplasie des cellules alpha, capteurs d’acides aminés, ce qui promeut la sécrétion d’insuline. Cette hyper-glucagonémie va diminuer la synthèse hépatique du glucose. C’est l’acide aminé arginine qui agirait à la fois sur la sécrétion de glucagon et d’insuline.
À retenir
La recherche est donc très active et porte l’espoir de tous de trouver des traitements ciblant les bases physiopathologiques de ces maladies dont la prévalence ne cesse d’augmenter que ce soit pour le DT1, le DT2 ou l’obésité.
L’auteur déclare ne pas avoir de liens d’intérêt avec cet article.