Association entre faible temps passé en normoglycémie et installation d’un dysfonctionnement cognitif ou de lésions hippocampiques chez les diabétiques de type 2
En Chine, la prévalence de la démence est de 6,0 % chez les personnes âgées de plus de 60 ans, mais elle ne concerne que 4,8 % des sujets non diabétiques alors qu’elle se chiffre à 10,2 % pour les diabétiques. De nombreuses publications ont déjà suggéré que pouvait exister un lien entre la diminution du temps passé en euglycémie et le risque de complications microvasculaires et macrovasculaires.
Cette présentation chinoise s’est donc intéressée à la potentielle relation entre la durée de l’euglycémie et l’apparition de dysfonctionnements cognitifs ou de lésions hippocampiques chez des patients diabétiques de type 2 (DT2).
L’étude
Pour cette étude ont été sélectionnés 520 participants DT2, âgés de plus de 45 ans (à l’exclusion des déments, des hypothyroïdiens et des sujets ayant eu des hypoglycémies sévères dans les 3 mois), pour réaliser une surveillance continue de la glycémie associée à des évaluations cognitives cliniques. L’observation en milieu hospitalier a été réalisée de janvier 2017 à avril 2022.
Parmi eux, 100 patients ont bénéficié en plus d’une imagerie par résonance magnétique pour évaluer les changements structurels et fonctionnels du cerveau (en se focalisant sur l’activation fronto-orbitale gauche et du gyrus cingulaire postérieur droit).
Les résultats
Une diminution du temps passé en euglycémie était associée à un déclin cognitif de la mémoire immédiate, du langage, de l’attention, de la mémoire retardée et de la vitesse de traitement.
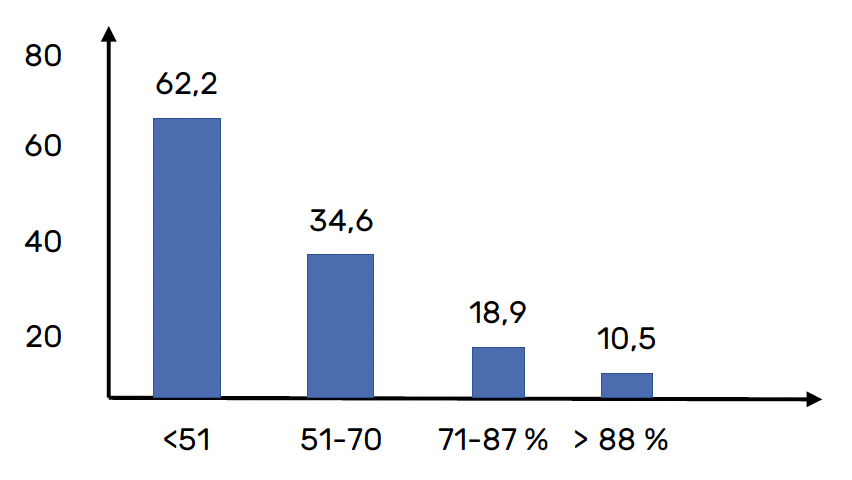
La prévalence des troubles cognitifs légers (MCI) s’est avérée significativement associée aux quartiles inférieurs de temps dans la norme (p < 0,001) (Fig. 1). Comparés aux patients qui restaient à plus de 88 % du temps dans la norme, ceux qui étaient en deçà de 51 % avaient un risque sept fois plus important de développer des troubles centraux ultérieurs.
Figure 1 – Pour chaque diminution de 10 % du temps en normoglycémie, le risque de MCI était augmenté de 1,36 fois (IC 95 % = 1,20-1,52).
Les odds ratios (OR) ajustés et multivariés de ces troubles cognitifs associés aux quartiles temps étaient les suivants :
• Q1 : ≥ 88 % = 1,0 ;
• Q2 : 71-87 % = 1,6 ;
• Q3 : 51-70 % = 3,02 ;
• Q4 : < 51 % = 7,67.
IRM
Les patients cognitivement normaux, mais présentant un faible temps en normoglycémie qui ont pu bénéficier d’une IRM, avaient une réduction du volume des sous-régions de l’hippocampe gauche et une diminution de l’activation du gyrus para-hippocampique droit.
Durant les 5 ans de surveillance exercée sur plus de 500 patients diabétiques de type 2, plus le temps passé dans la cible glycémique était faible, plus importante était la prévalence des troubles cognitifs. Pour ceux ayant bénéficié d’une imagerie IRM, il est probable que cette atteinte soit médiée par des lésions hippocampiques.
• Zhang Z, Yu C, Bi Y. Associations of lower time in range with cognitive dysfunction and hippocampal damage in adults with type 2 diabetes. EASD 2023 ; abst. 67.
Le jeûne chez le diabétique de type 2 provoque une diminution de la glycémie cérébrale et une augmentation de l’utilisation des acides gras
Depuis plusieurs années, des études épidémiologiques ont objectivé un risque plus important de développer une maladie d’Alzheimer chez les DT2. La maladie d’Alzheimer étant associée à un hypométabolisme cérébral, il a été émis l’hypothèse que la résistance tissulaire à l’insuline de ces patients induirait également un hypométabolisme cérébral et que ces altérations métaboliques centrales constitueraient un lien entre le DT2 et la maladie d’Alzheimer.
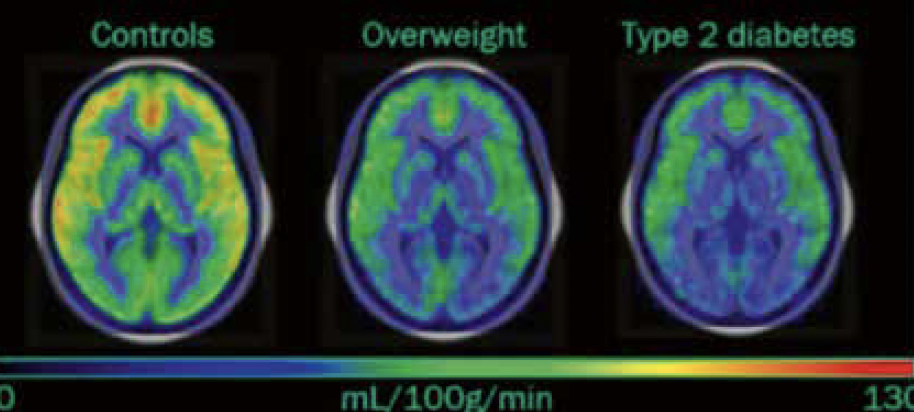
Cette présentation suédoise s’est ainsi intéressée, lors d’un jeûne, à l’utilisation du glucose cérébral chez des patients diabétiques et/ou obèses comparés à des sujets témoins, en utilisant l’imagerie TEP au [18F]FDG (un glucose radiomarqué) et au [18F]FTHA (un analogue d’acides gras radiomarqué).
L’étude
Entre décembre 2019 et juin 2022, 38 sujets ont ainsi été observés :
• 10 présentaient un DT2 (âge : 60,5 ans ; IMC : 33,6 kg/m2 ; 7 hommes ; HOMA-IR : 8,3) ;
• 13 souffraient d’une obésité, sans DT2 (âge : 56,3 ans ; IMC : 33,1 kg/m2 ; 3 hommes ; HOMA-IR : 4) ;
• 15 sujets maigres servaient de témoins (âge : 56,9 ans ; IMC : 22,6 kg/m2 ; 4 hommes ; HOMA-IR : 1,3).
Bien sûr, les sujets présentant déjà une maladie d’Alzheimer ou un dysfonctionnement cognitif (MMS < 27) ont été exclus de l’étude.
Les participants ont bénéficié d’une imagerie TEP cérébrale au [18F]FDG et au [18F]FTHA après 6 heures de jeûne, pour mesurer l’utilisation du glucose et des acides gras, à l’aide d’un système PET/IRM 3T.
La perfusion cérébrale a été évaluée par IRM associée à une mesure (par 1H-MRS) métabolique de N-acétyl aspartate, choline et myo-inositol dans les régions sélectionnées.
Par ailleurs, plusieurs marqueurs de neurodégénérescence cérébrale ont été prélevés dans le liquide céphalorachidien, notamment les protéines P-Tau, T-Tau, Abêta 1-40 et Abêta 1-42. Les sujets ont aussi été génotypés pour l’allèle APoE4.
Les résultats
Absorption du glucose et des acides gras
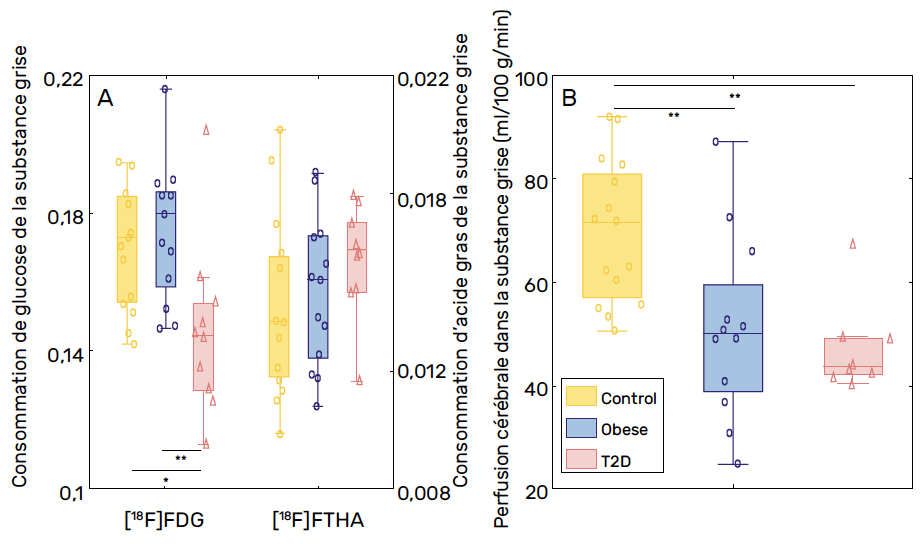
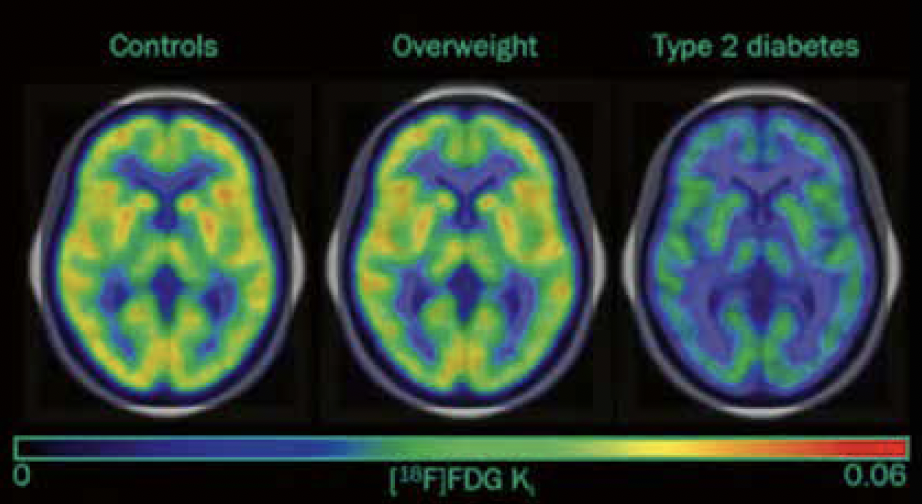
Juste après la période de jeûne, l’absorption de glucose dans la matière grise (GM) (Fig. 2A et 3) était plus faible chez les DT2 que chez les témoins (p = 0,01) et les participants obèses (p = 0,004). Elle était par ailleurs corrélée négativement à la résistance à l’insuline mesurée avec HOMA-IR (p < 0,05).
Figure 2 – A – Mesure de la consommation de glucose et d’acide gras dans les tissus cérébraux des sujets obèses et diabétiques. B – Mesure de la perfusion cérébrale dans la substance grise des sujets obèses et diabétiques.
Figure 3 – IRM de l’utilisation glucosée cérébrale chez les sujets contrôle, sujets obèses et sujets diabétiques de type 2.
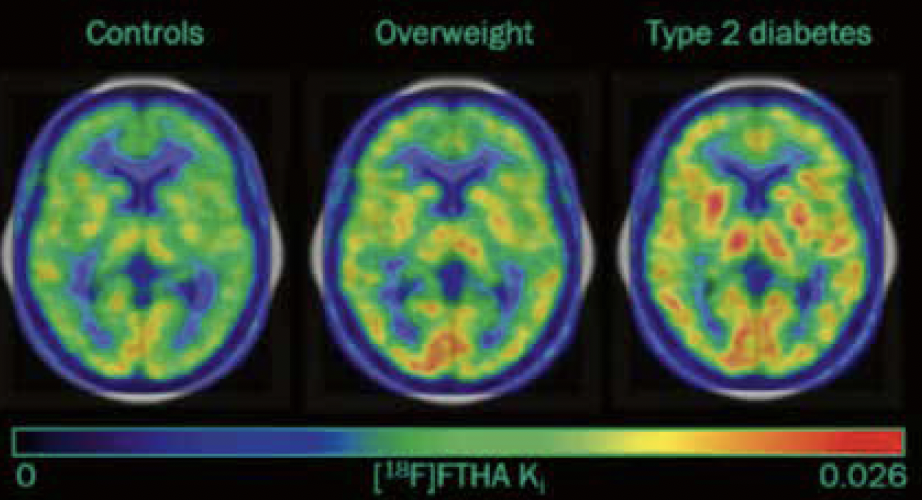
En revanche, le taux d’absorption des acides gras dans la substance blanche (MW) était plus élevé dans le groupe DT2 que dans le groupe témoin (p = 0,03). Aucune différence statistique n’a été trouvée dans la GM (Fig. 2A et 4).
Figure 4 – IRM de l’utilisation des acides gras cérébraux chez les sujets contrôle, sujets obèses et sujets diabétiques de type 2.
Perfusion cérébrale
La perfusion cérébrale était plus faible dans les deux parties, GM et MW, chez les DT2 (p = 0,003 et 0,01) et chez les obèses (p = 0,006 et 0,02) par rapport aux témoins (Fig. 2B et 5).
Figure 5 – IRM de la perfusion cérébrale chez les sujets contrôle, sujets obèses et sujets diabétiques de type 2.
Aucune différence n’a toutefois été observée s’agissant des métabolites étudiés par MRS ou sur les marqueurs du LCR.
Allèle APoE4
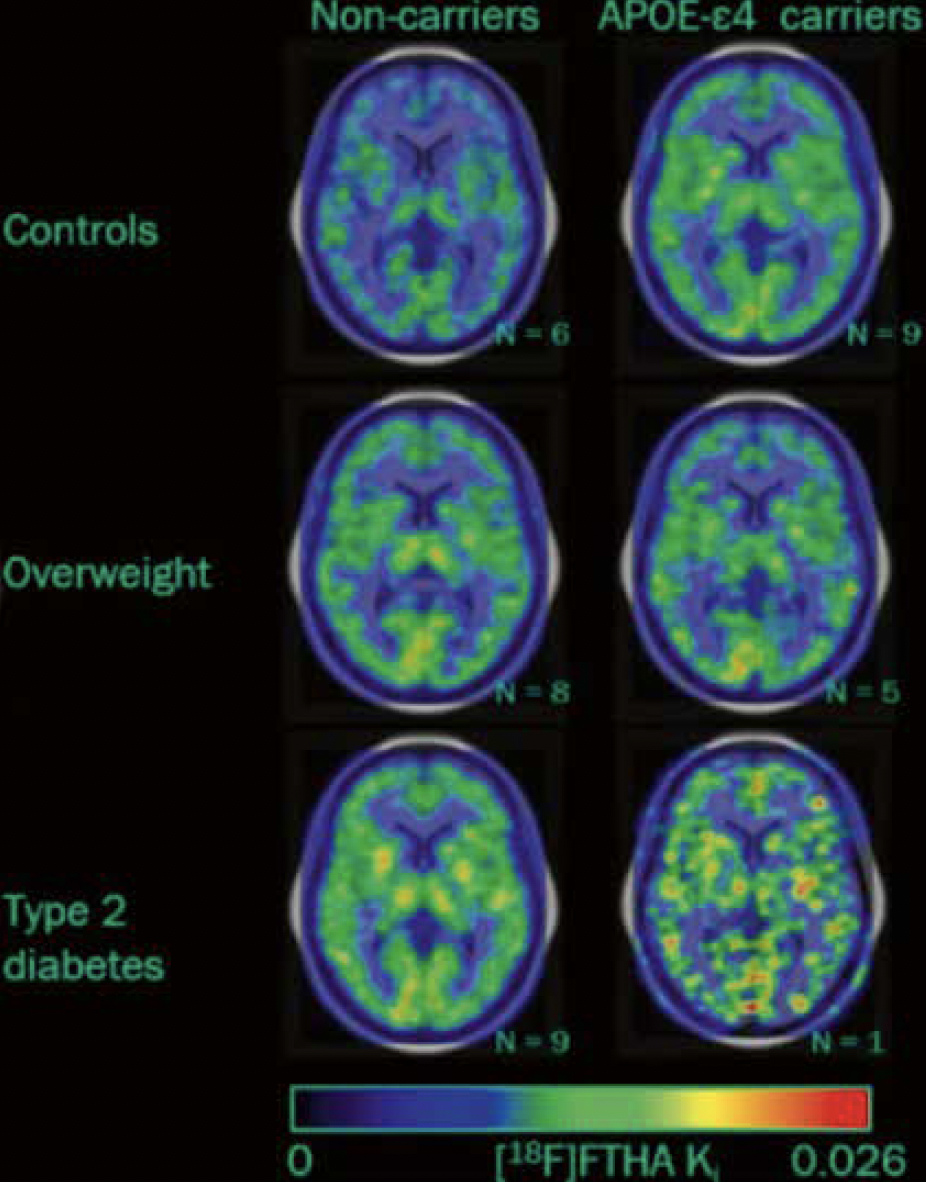
S’agissant des sujets qui possédaient le génotype de l’allèle APoE4, l’IRM a montré une forte distribution des acides gras intracérébraux, une accumulation parenchymateuse observée aussi bien chez les sujets contrôles que chez les DT2. En revanche, rien de tel n’a été observé avec les sujets obèses (Fig. 6).
Figure 6 – IRM de l’utilisation des acides gras cérébraux chez les sujets contrôle, sujets obèses et sujets diabétiques de type 2.
L’hypométabolisme cérébral du glucose pendant le jeûne est bien documenté dans la maladie d’Alzheimer. Dans cet esprit, cette étude de jeûne de 6 heures chez les 38 sujets, diabétiques, obèses et témoins, a montré que chez les DT2 sans déficience cognitive, l’utilisation du glucose cérébral était plus faible que chez les témoins non diabétiques et corrélée à la résistance périphérique à l’insuline.
La réduction du flux sanguin constatée par ailleurs pourrait être une conséquence de la moindre demande en oxygène suite à cette diminution de la consommation de glucose. L’absorption accrue d’acides gras pourrait alors constituer un mécanisme compensatoire.
Un suivi complémentaire des DT2 porteurs du gène APoE4 permettrait également de mesurer l’effet de ces hypo-consommations glucosées cérébrales sur l’apparition d’une maladie d’Alzheimer ultérieure.
• Schain M, Johansson E, Laitinen I et al. Decreased cerebral glucose and increased cerebral fatty acid utilisation during fasting in type 2 diabetes. EASD 2023 ; abst. 68.
Le cholestérol résiduel est un facteur de risque indépendant de démence chez les diabétiques de type 2 : étude de cohorte nationale
Aucune étude à ce jour n’a évalué longitudinalement l’effet du cholestérol résiduel sur l’incidence de la démence des patients atteints de DT2. Cette étude coréenne rétro-spective en a fait son objectif en recherchant un potentiel lien entre le taux de cholestérol résiduel de tels patients et l’apparition d’une démence.
L’étude
Ont donc été sélectionnés, au sein d’une très large cohorte nationale, 2 621 596 patients atteints de DT2, âgés de plus de 40 ans, ayant bénéficié d’un dépistage de santé entre 2009-2011 et qui ont été suivis jusqu’en 2020.
La méthode statistique a utilisé la régression de Cox pour calculer le risque (HR) de maladie d’Alzheimer et de démence vasculaire dans chaque quartile du cholestérol résiduel, en tenant compte des facteurs de risque conventionnels de démence vasculaire.
L’estimation du cholestérol résiduel, considéré comme plus athérogène que les autres apolipoprotéines, était fondée sur la formule : Remnant-c = cholestérol total-HDL-c – LDL-c.
Les résultats
Au cours du suivi médian de 10,3 ans, le développement :
• d’une démence toutes causes confondues a été constaté chez 146 991 (5,6 %) d’entre eux,
• d’une maladie d’Alzheimer chez 117 739 (4,5 %),
• d’une démence vasculaire chez 14 536 (0,6 %).
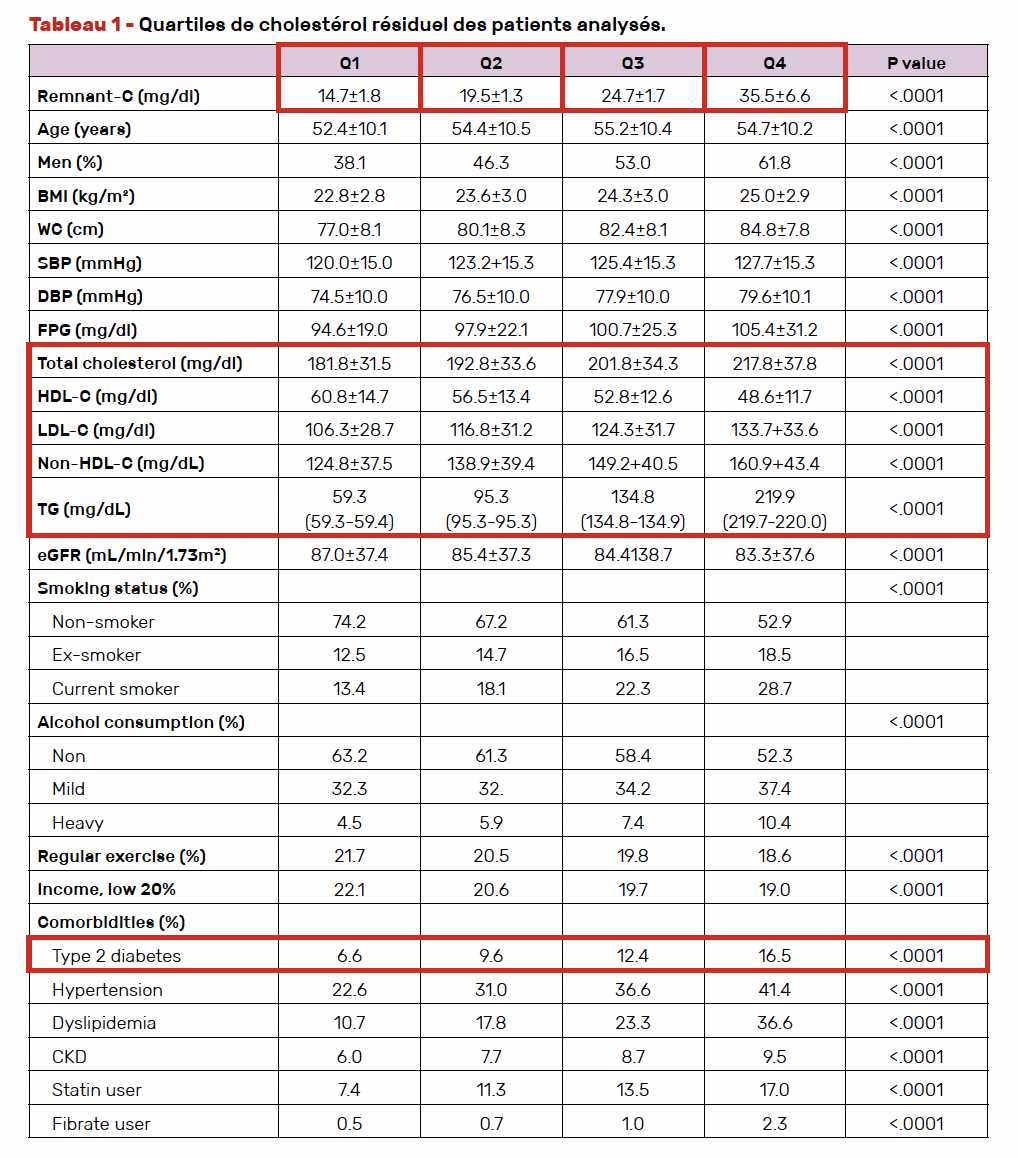
Le risque de démence augmentait progressivement avec les niveaux de cholestérol résiduel et les patients ont pu être répartis en quatre quartiles selon leur taux de cholestérol résiduel (Tab. 1).
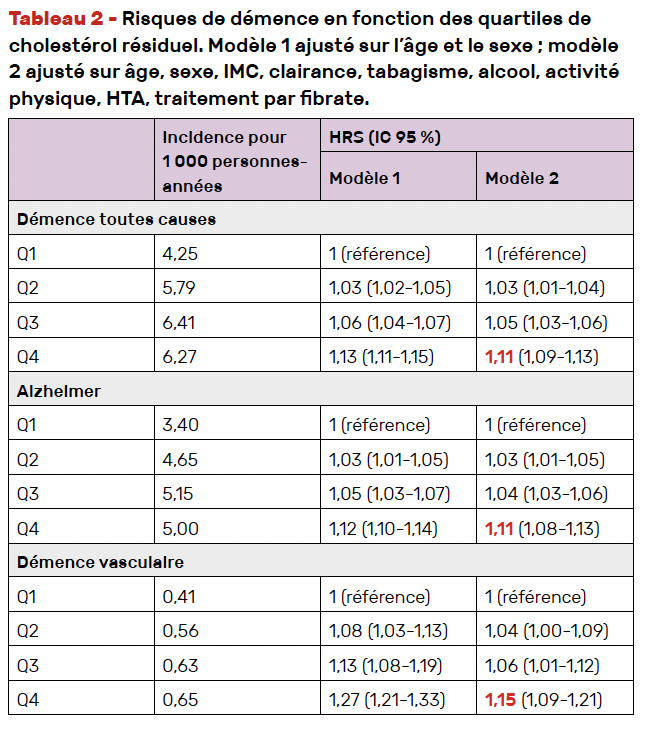
Les HR de développer une atteinte dégénérative centrale étaient significativement plus importants dans le quartile de Remant-c le plus élevé, s’agissant des trois pathologies retenues :
• pour toutes les causes de démence de 1,11,
• pour la maladie d’Alzheimer de 1,11,
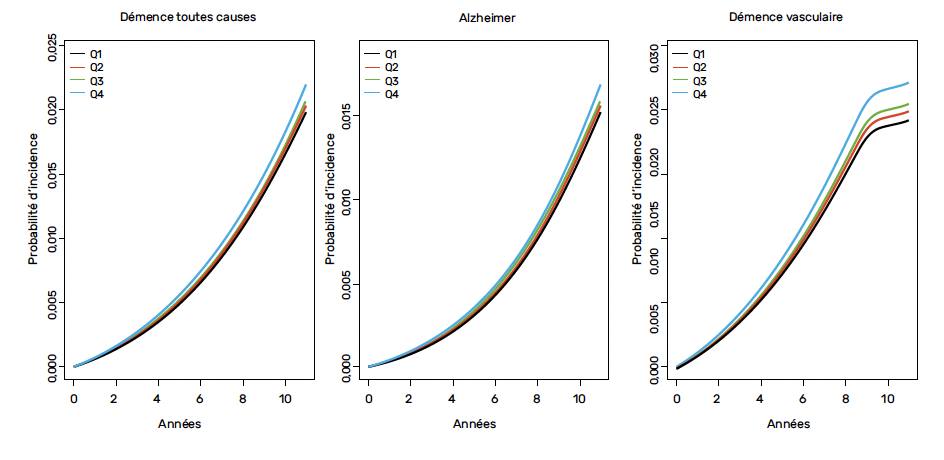
• pour la démence vasculaire de 1,15 (Tab. 2 et Fig. 7).
Figure 7 – Incidence cumulée de démence en fonction des quartiles de cholestérol résiduel.
Par ailleurs, le risque accru de démence associé à un cholestérol résiduel élevé était plus prononcé chez les patients jeunes :
• chez les 40-49 ans, HR pour la démence toutes causes confondues : 1,52,
• chez les 50-59 ans, HR : 1,17,
• chez les 60-69 ans, HR : 1,11,
• chez ≥ 70 ans, HR : 1,08.
Dans cette étude observationnelle coréenne de patients DT2, plus le taux de cholestérol résiduel était élevé, plus le risque de démence était accru. Ce lien était indépendant des facteurs de risque traditionnels de démence et était plus prononcé chez les patients les plus jeunes.
• Jung H, Huh J, Rho E et al. Remnant cholesterol is an independent risk factor for dementia in patients with type 2 diabetes: a nationwide population-based cohort study. EASD 2023 ; abst. 71.
Évaluation des facteurs contribuant à la diminution du risque d’accident vasculaire cérébral chez des diabétiques de type 2 au cours des dernières décennies : l’étude Fremantle Diabetes
L’étude Fremantle Diabetes a montré dans des publications précédentes que l’incidence sur 5 ans des accidents vasculaires cérébraux avait diminué de moitié au cours des 15 années séparant sa première phase d’observation (FDS1) de sa seconde phase (FDS2).
Cette communication australienne s’est focalisée sur l’effet que les facteurs de risque de maladies cérébrovasculaires pouvaient avoir sur ces constats.
L’étude
Les DT2 recrutés dans FDS1 entre 1993 et 1996 (n = 1 426 ; âge moyen 64 ans, 49 % d’hommes ; durée de diabète 4 ans) puis dans FDS2 entre 2008 et 2011 (n = 1 732 ; âge moyen 65 ans, 52 % d’hommes ; durée de diabète 8 ans) ont été suivis sur 10 ans dès leur première hospitalisation pour un accident vasculaire cérébral.
Les risques d’accidents vasculaires cérébraux ont été calculés par régression de Cox (HR) dans FDS1, dans FDS2 et dans la cohorte combinée. L’hypothèse des risques proportionnels a été évaluée et éventuellement ajustée par des covariables significatives.
Les résultats
Dans FDS1 ont été signalés 132 AVC (10,2 %) alors que, dans FDS2, seuls 85 AVC (5,8 %) ont été enregistrés. L’incidence sur 10 ans (IRs) des accidents vasculaires cérébraux dans le FDS1 était de 12,4/1 000 personnes-années versus 6,6 dans FDS2 avec un ratio RR de 0,54 pour FDS1 versus 0,55 pour FDS2 (p < 0,001).
Les facteurs de risque potentiels
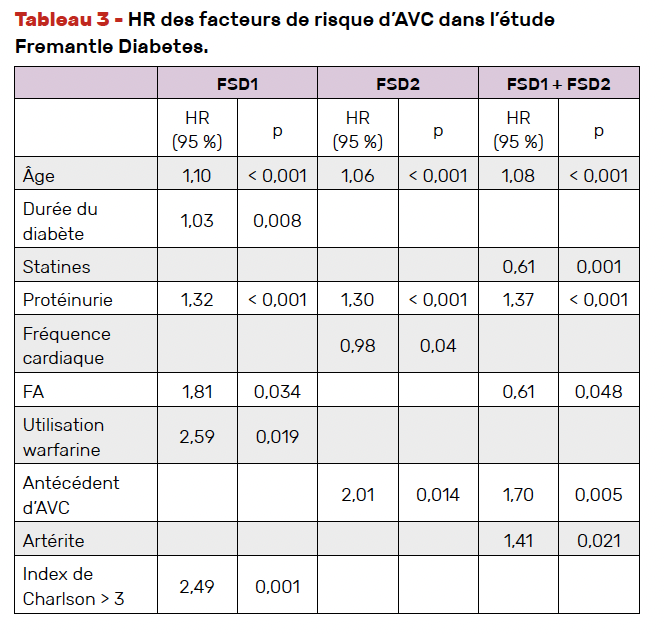
Les facteurs de risque enregistrés comme potentiels liens avec le premier accident vasculaire cérébral sont indiqués dans le tableau 3.
D’évidence dans les deux groupes FDS1 et FDS2, quelle que soit l’année de prise en compte, les facteurs de risque d’un AVC statistiquement significatifs étaient l’augmentation de l’âge et la protéinurie (uACR).
Lorsque l’analyse se porte spécifiquement sur chacun des groupes, d’autres facteurs peuvent être retenus :
• dans FDS1 : la fibrillation/flutter auriculaire (FA), l’utilisation de warfarine et l’indice de comorbidité de Charlson4 (CCI) ≥ 3 ;
• dans FDS2 : la fréquence cardiaque et les antécédents de maladie cérébrovasculaire (AVC).
Dans la cohorte regroupée FDS1 + FDS2, l’âge avancé, la protéinurie, la FA et les maladies cardiovasculaires antérieures étaient des facteurs de risque d’AVC indépendants, tout comme l’utilisation de statines et la maladie artérielle périphérique.
Ces données à long terme confirment la réduction des accidents vasculaires cérébraux compliquant le diabète de type 2 et indiquent que la microalbuminurie et la FA restent des facteurs de risque potentiellement modifiables pour améliorer encore cette diminution.
• Davis WA, Gregg EW, Davis TME. Temporal trends in cardiovascular complications in people with or without type 2 diabetes: the Fremantle Diabetes study. J Clin Endocrinol Metab 2020 ; 105 : dgaa215.
• Davis WA, Hellbusch V, Hunter ML et al. Contemporary cardiovascular risk assessment for type 2 diabetes including heart failure as an outcome: the Fremantle Diabetes study phase II. J Clin Med 2020 ; 9 : 1428.
• Davis WA TME, Davis WA et al. An assessment of factors contributing to the decline in risk of stroke complicating type 2 diabetes over recent decades: the Fremantle Diabetes Study. EASD 2023 ; abst. 72.