L’essentiel en un clin d’œil
• Effet rénal des inhibiteurs du SGLT2 comparés aux agonistes du récepteur du GLP-1 chez le diabétique de type 2 : l’étude DARWIN-Renal.
• Effets du sémaglutide, de l’empagliflozine et de leur association sur l’IRM pondérée en diffusion rénale et le volume rénal des diabétiques de type 2.
• Effet de l’empagliflozine sur l’excrétion urinaire d’albumine et les biomarqueurs des lésions hypoxiques de la maladie rénale diabétique en phase précoce : étude EUROBEAT.
• La canagliflozine améliore la ferroptose des podocytes diabétiques.
• Le bypass gastrique et la gastrectomie longitudinale améliorent l’albuminurie plus que le traitement médical à base de iSGLT2 ou GLP-1RA, lors d’un essai clinique randomisé.
TOP 5 – Effet rénal des inhibiteurs du SGLT2 comparés aux agonistes du récepteur du GLP-1 chez le diabétique de type 2 : l’étude DARWIN-Renal
Cause d’insuffisance fonctionnelle chronique et de risques cardiovasculaires, l’altération rénale progressive induite par le diabète a été surveillée par l’étude DARWIN-Renal. L’université italienne de Padoue nous a présenté quelques résultats s’agissant de la filtration glomérulaire estimée (DFGe) et de l’albuminurie de diabétiques de type 2 (DT2) traités soit par des inhibiteurs du co-transporteur sodium-glucose 2 (iSGLT2), soit par des agonistes du récepteur du peptide-1 de type glucagon (GLP-1RA).
L’étude observationnelle DARWIN-Renal
Cette étude observationnelle rétrospective multicentrique fut menée dans 50 sites, colligeant une cohorte de 48 593 patients sur la base de leurs dossiers médicaux électroniques. Les caractéristiques des patients, appariés par score de propension en sous-groupes de 5 701, étaient les suivantes : 61 % d’hommes, âgés de 61 ans, durée de diabète de 10 ans, HbA1c de 8,0 %, IMC moyen de 33 kg/m², 23 % en insuffisance rénale chronique (IRC).
Les traitements associés étaient pour 84 % de la metformine ; 23 % de l’insuline basale, 11 % des sulfamides, 3 % de la pioglitazone, 3 % des bolus insuliniques.
Les iSGLT2 proposés étaient la dapagliflozine (52,8 %), l’empagliflozine (38,5 %), la canagliflozine (8,5 %) et l’ertugliflozine (< 0,1 %). Les GLP-1RA étaient la dulaglutide (52,3 %), le liraglutide (30,8 %), l’exénatide (10,7 %), le sémaglutide (3,8 %) et le lixisénatide (2 %).
Les résultats
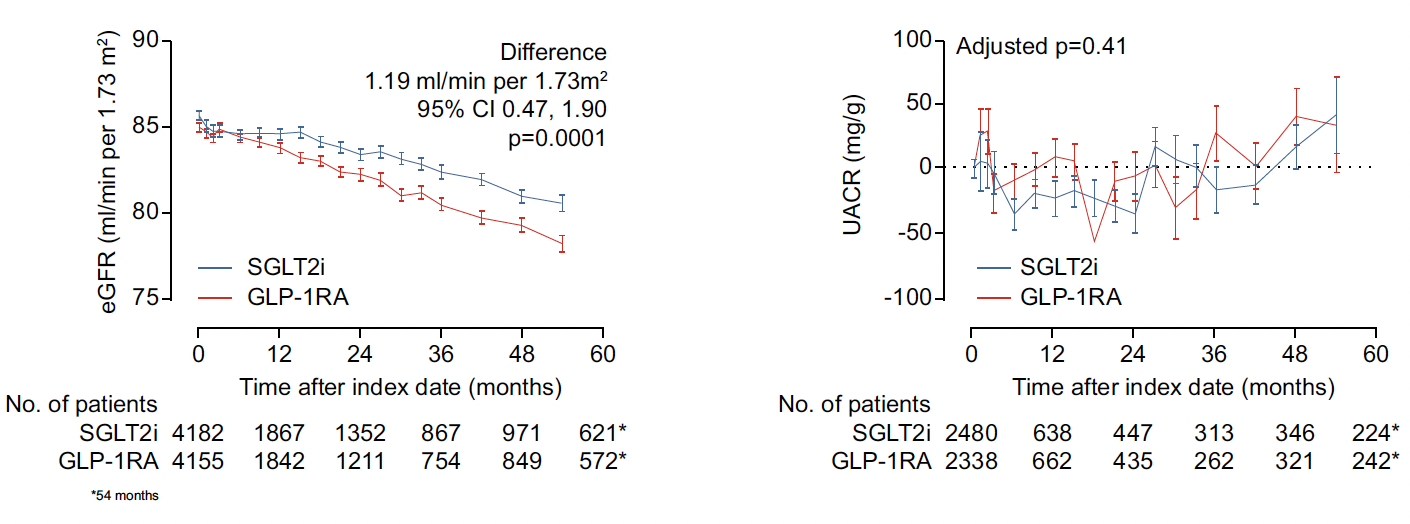
Après 2,2 ans d’observation, la baisse du DFGe était plus faible de 1,19 ml/min (p = 0,001) dans le groupe iSGLT2 comparé au groupe GLP-1RA, tandis que la variation de l’albuminurie n’était pas différente entre les groupes (Fig. 1).
Figure 1 – L’iSGLT2 altère moins la clairance que les GLP-1RA sans différence sur la microalbuminurie.
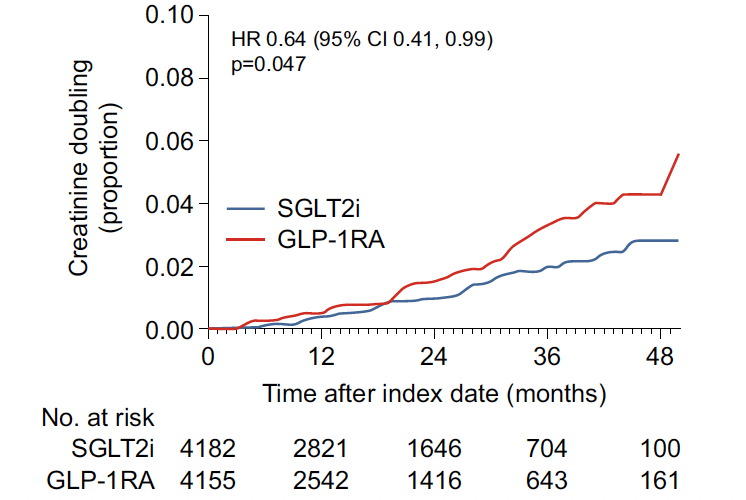
De la même manière, l’augmentation de la créatinine était plus faible dans le groupe iSGLT2 (HR 0,64 ; p = 0,047) comparé au groupe GLP-1RA (Fig. 2).
Figure 2 – Taux de doublement de la créatinine sous iSGLT2 et GLP-1RA.
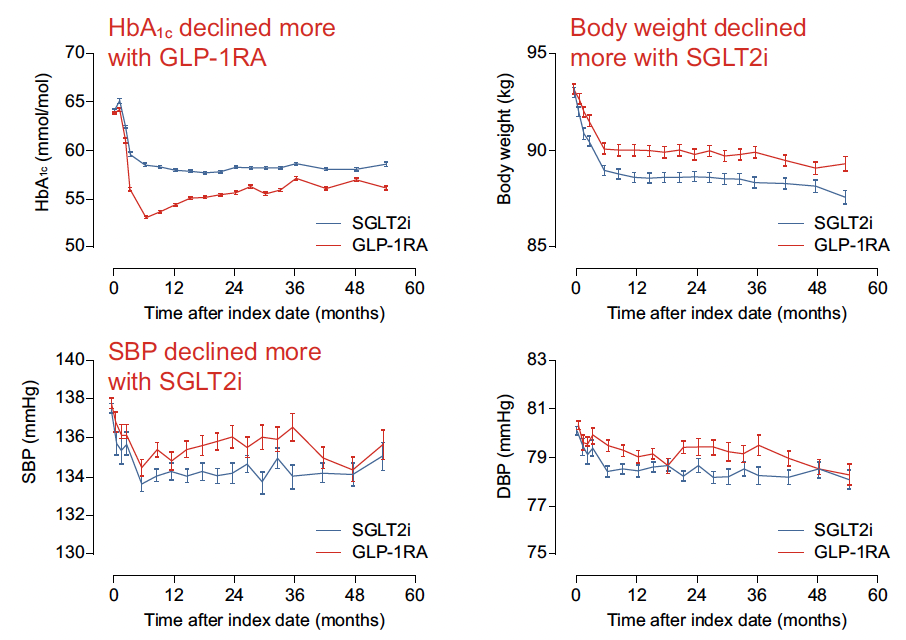
En matière de critères secondaires, le groupe sous iSGLT2 a vu baisser l’HbA1c de 0,2 %, le poids de 1,3 kg et la pression artérielle systolique de 1,1 mmHg, par rapport à celui sous GLP-1RA (Fig. 3).
Figure 3 – Diminution de l’HbA1c meilleure sous GLP-1RA ; perte de poids et baisse de la pression artérielle meilleures sous iSGLT2.
La supériorité du iSGLT2 dans la préservation du DFGe a été confirmée chez les patients sans IRC initiale (n = 4 416/groupe).
À retenir
Chez les DT2, un traitement par iSGLT2 a été associé à de meilleurs résultats rénaux comparé au GLP-1RA, tant en matière de ralentissement de la dégradation du DFGe, qu’en prévention primaire.
• Fadini GP, Morieri ML, Solini A et al. Comparative renal outcomes of matched cohorts of patients with type 2 diabetes receiving SGLT-2 inhibitors or GLP-1 receptor agonists under routine care: the DARWIN-Renal study. EASD 2024 : #1.
TOP 4 – Effets du sémaglutide, de l’empagliflozine et de leur association sur l’IRM pondérée en diffusion rénale et le volume rénal des diabétiques de type 2
Cette étude danoise s’est intéressée aux effets protecteurs des iSGLT2 sur la maladie rénale des diabétiques par le biais d’une IRM pondérée en diffusion (IRM-DWI), une mesure de la diffusion de l’eau proposée comme reflet de la microstructure rénale et de la fibrose rénale.
L’effet du sémaglutide, de l’empagliflozine et de leur association sur le coefficient de diffusion apparent rénal (ADC) et le volume rénal total (VRT) a ainsi été analysé au sein d’un essai clinique randomisé.
Une étude avec quatre groupes de traitement
Pendant 32 semaines, 80 DT2 de plus de 50 ans présentant un risque élevé de maladie cardiovasculaire ont été randomisés en quatre groupes de 20 patients pour recevoir un placebo, du sémaglutide, de l’empagliflozine ou leur combinaison.
L’analyse des effets du traitement a porté sur les changements de l’ADC (cortical, médullaire et ΔADC (ADC médullaire soustrait de l’ADC cortical)), ainsi que sur le VRT mesuré par IRM.
Les résultats
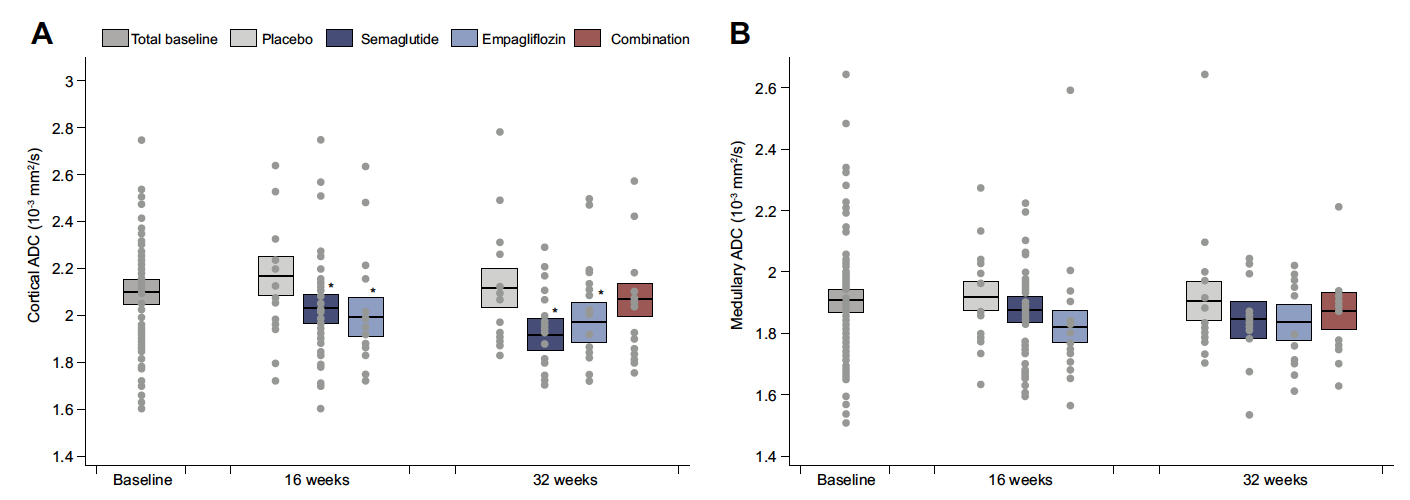
L’ADC cortical sous sémaglutide et empagliflozine a significativement diminué comparé au placebo (sémaglutide -0,20 x 10-3 mm2/s ; p < 0,001 / empagliflozine -0,15 x 10-3 mm2/s ; p = 0,01), mais aucun changement n’a été observé dans le groupe combiné (-0,05 x 10-3 mm2/s ; p = 0,29) par rapport au placebo. Ces changements n’étaient pas associés à des changements du DFG, de l’albuminurie, de la VRT ou des marqueurs de l’inflammation. L’ADC médullaire n’a été modifié dans aucun des groupes (Fig. 4).
Figure 4 – A. Diminution de la diffusion rénale corticale sous sémaglutide et empagliflozine séparément, mais pas en traitement combiné. B. Pas de modification de la diffusion rénale médullaire sous aucune forme de traitement comparé au placebo.
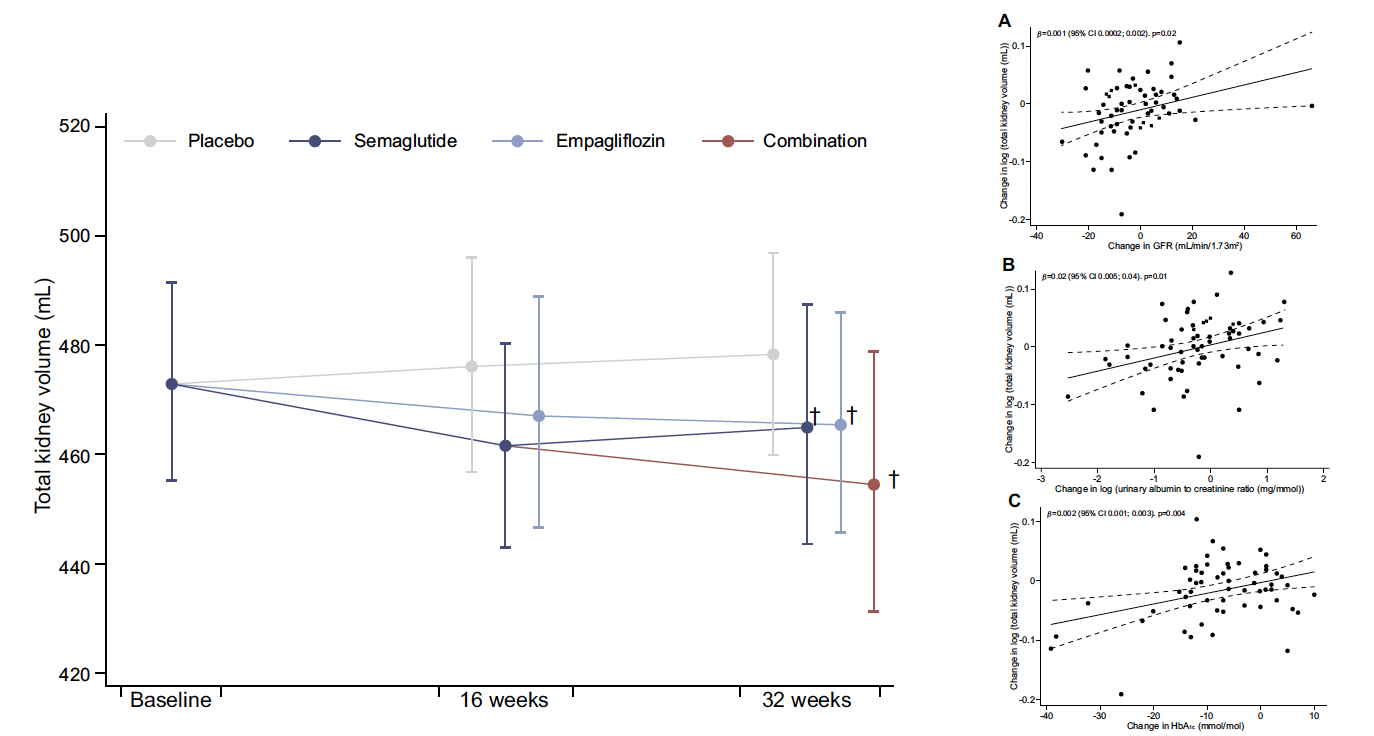
La ΔADC par rapport au placebo n’a été modifiée que par le sémaglutide (-0,13 x 10-3 mm2/s (p = 0,01). Le VRT a diminué de 3 % (p = 0,04) sous sémaglutide ; de 3 % (p = 0,02) sous empagliflozine et de 5 % (p < 0,001) dans le groupe combiné. Les réductions de la VTR ont été associées à des réductions du DFG, de l’albuminurie et de l’HbA1c (Fig. 5).
Figure 5 – Diminution du volume total rénal sous sémaglutide, empagliflozine et combinaison en lien avec les changements de clairance (A), de la microalbuminurie (B) et de l’HbA1c (C).
À retenir
Chez les DT2, le sémaglutide et l’empagliflozine réduisent le coefficient de diffusion apparent rénal cortical par rapport au placebo, indiquant des changements microstructurels rénaux, indépendants du DFG, de l’albuminurie ou de l’inflammation. La diminution du volume rénal total dans tous les groupes de traitement actif est probablement le fait d’une réduction de l’hyperfiltration.
• Vernstrøm L, Gullaksen S, Sørensen S et al. Effects of semaglutide, empagliflozin and their combination on renal diffusion-weighted magnetic resonance imaging and total kidney volume in patients with type 2 diabetes. EASD 2024 : #3.
TOP 3 – Effet de l’empagliflozine sur l’excrétion urinaire d’albumine et les biomarqueurs des lésions hypoxiques de la maladie rénale diabétique en phase précoce : étude EUROBEAT
Cette présentation japonaise s’est focalisée sur les effets réno-protecteurs des iSGLT2 à l’égard de la maladie rénale diabétique (MRD), en étudiant notamment son action sur la microalbuminurie, témoin probable de la réduction des facteurs angiogéniques induits par l’hypoxie rénale.
L’étude multicentrique EUROBEAT
Dans cet essai multicentrique, prospectif, en double aveugle, les DT2 avec microalbuminurie (rapport albumine/créatinine urinaire ; ACR : 30-299 mg/gCr) et débit de filtration glomérulaire (eGFR) > 30 ml/min, ont été randomisées pour recevoir de l’empagliflozine (10 mg/jour) (n = 40) ou un placebo (n = 39).
Le critère d’évaluation principal était la modification de l’ACR et de l’excrétion urinaire de la protéine de liaison aux acides gras de type hépatique (LFABP) entre le début et la 24e semaine. Le critère secondaire majeur était la modification des taux sériques de facteur de croissance endothélial vasculaire (VEGF), de protéine de type angiopoïétine 2 (ANGPTL2), de protéine de type angiopoïétine 4 (ANGPTL4) et d’adrénomédulline entre le début et la 24e semaine.
Les résultats
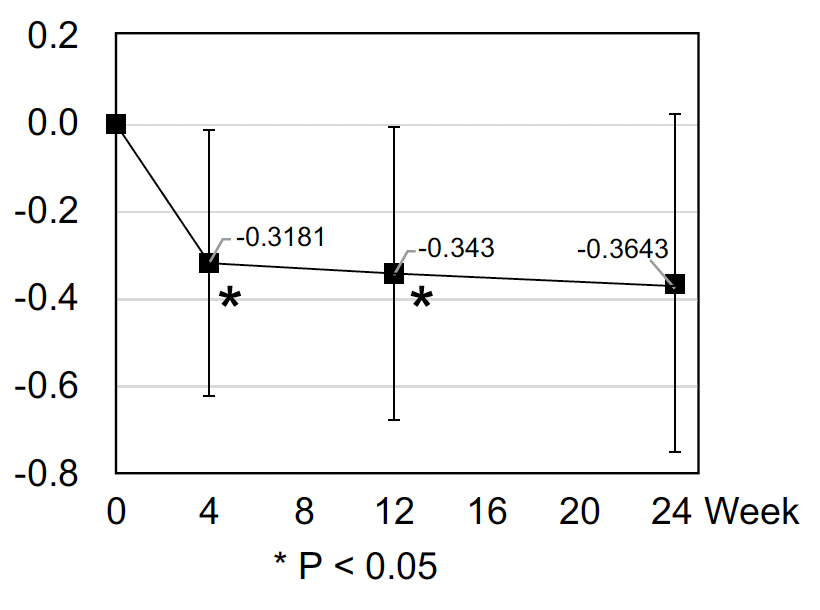
Bien que le log ACR ait diminué dans le groupe empagliflozine à 4 et 12 semaines, la différence de changement à 24 semaines entre les deux groupes n’était pas significative (-0,364 mg/gCr ; p = 0,0686) (Fig. 6).
Figure 6 – Logarithme de la diminution de la microalbuminurie sous empagliflozine versus placebo, diminué à 4 et 12 semaines, mais non significatif à 24 semaines.
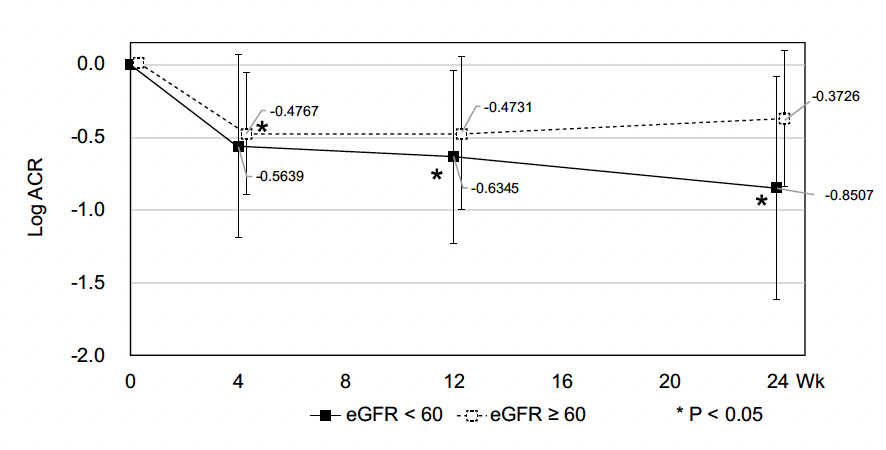
Lorsque le DFGe était < 60 ml/min, la réduction du log ACR était plus importante dans le groupe empagliflozine que dans le groupe placebo (-1,497 mg/gCr, IC versus -0,747 ; p = 0,003), mais lorsque le DFG était > 60 ml/min, la réduction du log ACR, bien que plus importante dans le groupe empagliflozine que dans le groupe placebo, n’était pas statistiquement significative (Fig. 7).
’
Figure 7 – Logarithme de la diminution de la microalbuminurie sous empagliflozine versus placebo selon le débit de filtration rénal.
Le VEGF et l’ANGPTL2 sériques ont diminué significativement dans le groupe empagliflozine (-76,088 versus -39,668 pg/ml ; p = 0,0332, pour le premier et -1,023 versus -0,532 pg/ml ; p = 0,0344 pour le second), mais il n’y avait pas de différence significative entre les groupes empagliflozine et placebo s’agissant de l’adrénomédulline, de l’ANGPTL4 et de l’excrétion urinaire de LFABP.
À retenir
Lors de l’étude japonaise EUROBEAT, le traitement par empagliflozine a diminué le rapport albumine/créatinine urinaire dans la maladie rénale diabétique avec microalbuminurie. Dans le même temps, la molécule a diminué le VEGF et l’ANGPTL2, ce qui pourrait donc contribuer aux mécanismes des effets néphroprotecteurs de cet agent.
• Makino H, Park H, Chen Q et al. Effect of empagliflozin on urinary albumin excretion and hypoxic injury biomarkers of early phase diabetic kidney disease (EUROBEAT study). EASD 2024 : #6.
TOP 2 – La canagliflozine améliore la ferroptose des podocytes diabétiques
Connue depuis 2012, la ferroptose a été surtout étudiée en oncologie et en neurologie, notamment dans les maladies neurodégénératives. Mais cette mort cellulaire par la peroxydation lipidique dépendante du fer a aussi été évoquée dans la pathogenèse des lésions des podocytes de la maladie rénale diabétique (MRD). L’effet bénéfique de la canagliflozine (CANA) sur la préservation des podocytes rénaux indépendamment du glucose pourrait bien être médié par des nanovésicules extracellulaires (EV), dérivées de cellules épithéliales tubulaires proximales (PTEC). L’étude de leur rôle dans la résistance des podocytes diabétiques à la ferroptose a donc fait l’objet de cette étude.
Une étude chinoise
Cette étude in vitro a co-cultivé une lignée cellulaire épithéliale tubulaire rénale proximale humaine (HK-2) avec une lignée cellulaire de podocytes rénaux humains (HPC). Fut ensuite administrée de la canagliflozine puis les EV du milieu de culture ont été isolées des cellules HK-2 par ultracentrifugation. Pour analyser la molécule candidate influençant la sécrétion d’EV par les PTEC après traitement par CANA, 40 souris mâles db/db âgées de 8 semaines ont été réparties au hasard dans quatre groupes : MRD, CANA à faible dose, CANA à forte dose et GW4869 ; 10 souris mâles db/m âgées de 8 semaines ont fait office de groupe témoin normal.
Les résultats
Après 12 semaines, la CANA (10 μM) a augmenté le nombre, mais pas la taille, des EV sécrétées par les cellules HK-2 dans un environnement à forte teneur en glucose (CH-EV), et les vésicules ont été absorbées par les podocytes. La CANA a réduit les niveaux de glucose sanguin, de créatinine et le rapport albumine-créatinine urinaire (UACR) chez les souris db/db (p < 0,05). Elle a également régulé à la baisse les niveaux d’expression de GPX4 et SLC7A11. L’UACR n’a, en revanche, pas été amélioré après l’association CANA/GW4869. L’amélioration de l’activité transcriptionnelle de FOXO1 par la CANA a entraîné une augmentation de la sécrétion d’EV par les cellules HK-2 en régulant à la hausse l’expression de VPS53, indiquant une relation de liaison directe entre FOXO1 et VPS53.
Les analyses protéomiques et lipidomiques révèlent un lien entre CH-EV et ferroptose ; elles suggèrent que la CANA module l’homéostasie lipidique des podocytes en modifiant la composition lipidique des EV.
La régulation négative de PCBP1, observée dans les cellules HPC cultivées dans des conditions de glucose élevé, se corrige après traitement par CH-EV. Cette diminution de l’expression de PCBP1 dans les cellules HPC augmente les niveaux d’ACSL4, améliore la ferroptose dans ces cellules et stabilise l’ARNm.
À retenir
La canagliflozine améliore la production et la sécrétion des nanovésicules extracellulaires dérivées de cellules épithéliales tubulaires proximales grâce à la régulation positive de l’axe FOXO1-VPS53. Elle améliore les podocytes diabétiques en modulant la teneur en nanovésicules pour atténuer la ferroptose.
• Dixon SJ, Lemberg KM, Lamprecht MR, Skouta R. Ferroptosis: an iron-dependent form of nonapoptotic cell death. Cell 2012 ; 149 : 1060-72.
• Qun G, Wei F, Luo F et al. Extracellular vesicles as messengers: how canagliflozin improves diabetic podocytes ferroptosis.EASD 2024 : #2.
TOP 1 – Le bypass gastrique et la gastrectomie longitudinale améliorent l’albuminurie plus que le traitement médical à base de iSGLT2 ou GLP-1RA, lors d’un essai clinique randomisé
Le consensus ADA/EASD recommande l’utilisation d’iSGLT2 et de GLP-1RA chez les DT2 atteints d’insuffisance rénale chronique (IRC). Par ailleurs, la chirurgie bariatrique, notamment le bypass gastrique (GB) et la gastrectomie longitudinale (SG), a montré des effets bénéfiques sur l’albuminurie.
Cette étude chilienne s’est donc attachée, chez des patients atteints d’IRC, de DT2 et obèses de grade I, à comparer l’effet de la chirurgie bariatrique à la combinaison thérapeutique iSGLT-2 et GLP-1RA (MED).
L’étude PRODIGIES
Cet essai contrôlé, prospectif, a recruté des patients DT2 dont l’IMC était compris entre 30 et 35 kg/m2 et souffrant d’une IRC (rapport albumine-créatinine urinaire [UACR] > 30 mg/g). La randomisation a inclus 24 patients en GB ; 24 en SG et 23 en MED.
Les caractéristiques initiales des patients des trois groupes étaient comparables : âge (51,9 ans pour GB ; 51,5 ans pour SG ; 54,9 ans pour MED) ; IMC (32,2 kg/m2 pour GB ; 31,6 kg/m2 pour SG ; 31,3 kg/m2 pour MED) et HbA1c (9,0 % pour GB ; 9,3 % pour SG ; 9,1 % pour MED). L’UACR initial et l’eGFR étaient de 96,0 mg/g et de 95,7 ml/min dans le groupe GB ; 59,1 mg/g et 95,4 ml/min dans le groupe SG ; 98,0 mg/g et 93,4 ml/min dans le groupe MED.
Les résultats
Après 12 mois de suivi, dans le groupe MED, 6/24 patients étaient sous GLP-1RA seul, 1/24 sous iSGLT2 seul et 16/24 sous l’association GLP-1 et iSGLT2. Dans le groupe chirurgical SG, 4/24 patients ont utilisé un iSGLT2. Aucun patient chirurgical (SG et GB) n’a utilisé de GLP-1RA.
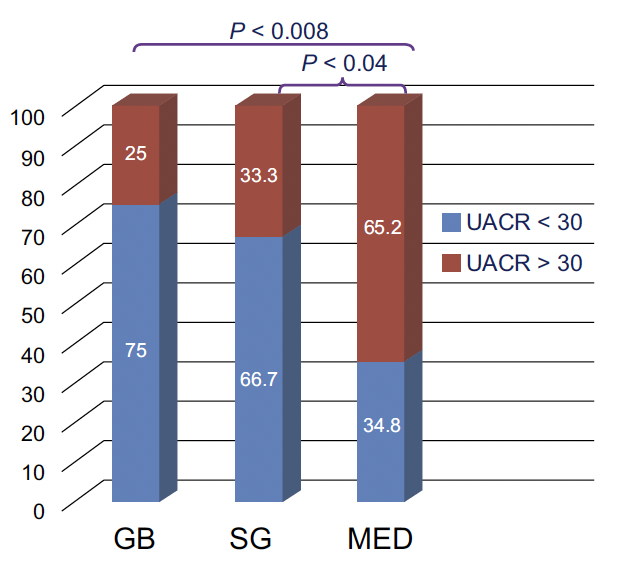
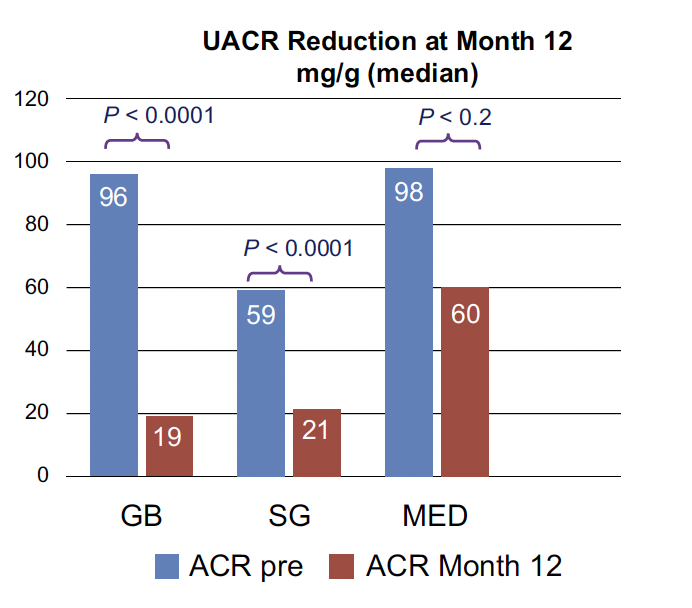
Une diminution de l’albuminurie a été observée chez 75 % des patients après GB, 66,7 % après SG et 34,8 % après MED (p = 0,03) (Fig. 8A). La réduction de l’UACR était de 97,1 mg/g dans le groupe GB (p < 0,0001) ; 80,3 mg/g dans le groupe SG (p < 0,0001) et 20,2 mg/g dans le groupe MED (p = 0,2) (Fig. 8B).
Figure 8A – Réduction de l’albuminurie.
Figure 8B – Réduction du rapport albumine-créatinine urinaire.
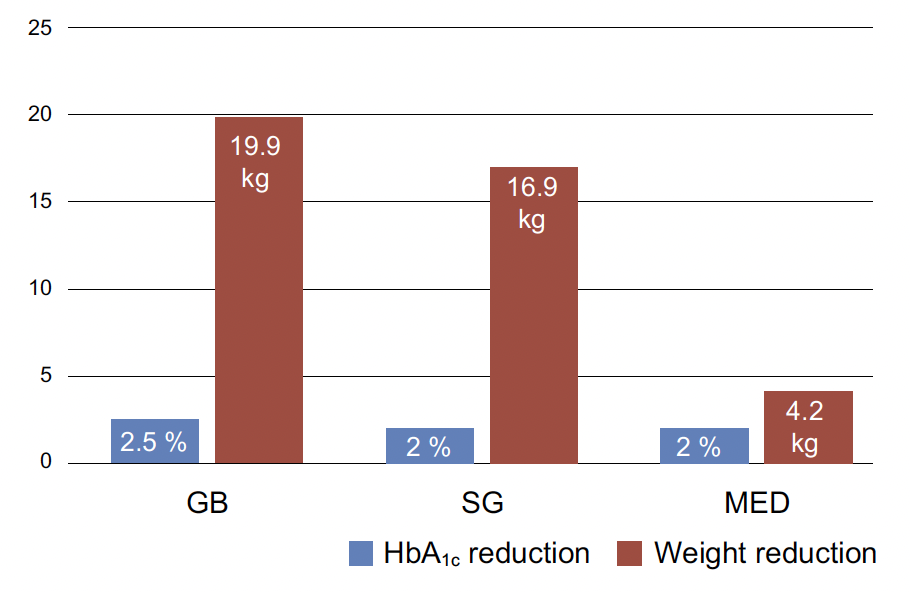
La perte de poids était plus importante dans les groupes chirurgicaux que dans le groupe MED, sans différence entre GB et SG (-19,9 kg dans le groupe GB, p < 0,0001 ; -16,7 kg dans le groupe SG, p < 0,0001 ; -4,3 kg dans le groupe MED, p = 0,3). La réduction de l’HbA1c était similaire entre les trois groupes (-2,5 % dans le groupe GB ; -2,0 % dans le groupe SG ; -2,1 % dans le groupe MED ; p < 0,0001 pour tous les groupes) (Fig. 9).
Figure 9 – Réduction du poids et de l’HbA1c sous les trois traitements : bypass (GB), sleeve (SG) et médical.
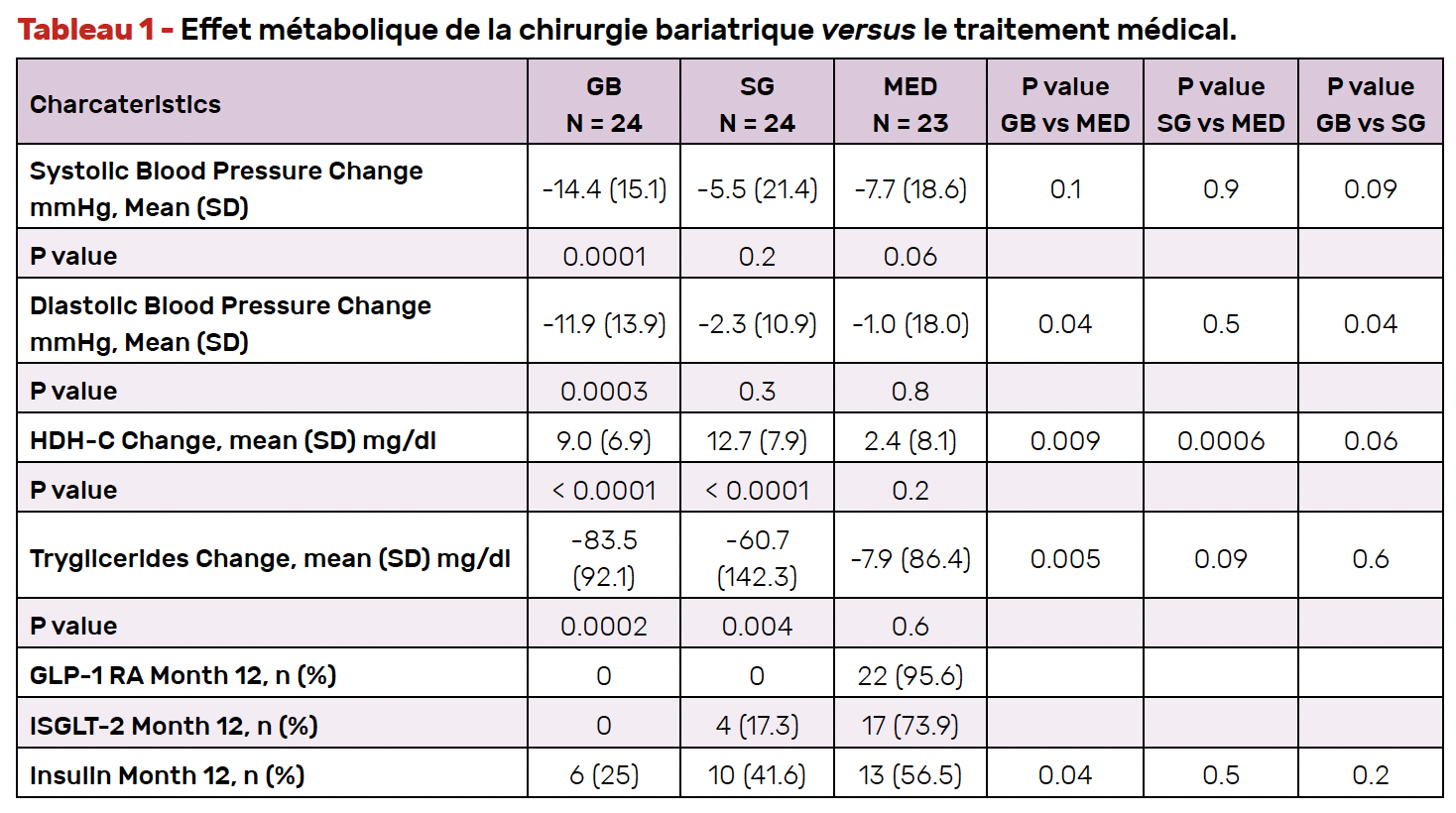
Au plan métabolique, l’effet positif était plutôt en faveur de la chirurgie, tandis que seul le bypass agissait efficacement sur la pression artérielle en diminuant la systolique de 14,4 versus 5,5 mmHg pour SG et 7,7 mmHg pour MED (Tab. 1).
Il y a eu trois complications chirurgicales : une fuite avec septicémie chez un patient GB, une perforation intestinale et une thrombose mésentérique chez deux patients SG. Tous les patients ont bénéficié d’une récupération complète. Aucun effet indésirable grave n’est survenu chez les patients MED.
À retenir
Après 12 mois de suivi, la chirurgie bariatrique a amélioré l’albuminurie des patients diabétiques de type 2, obèses de grade I, atteints d’IRC, mieux que le traitement médical. C’est l’ampleur de la perte de poids, et non les changements d’HbA1c ou de pression artérielle, qui était associée à cette amélioration de l’albuminurie.
• Valderas J, Boza C, le Roux C. Gastric bypass and sleeve gastrectomy improve albuminuria more than iSGLT-2/GLP-1RA based medical therapy: a randomised clinical trial. EASD 2024 : #4.
L’auteur déclare ne pas avoir de liens d’intérêt en rapport avec cet article.