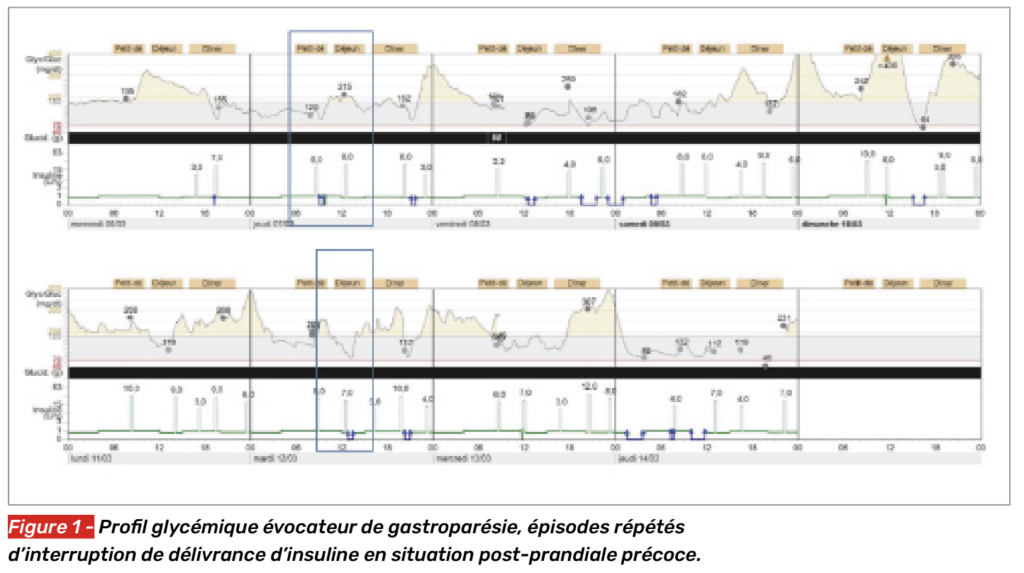
Le retentissement clinique et/ou glycémique du retard de vidange de l’estomac peut être très hétérogène en fonction des patients. Dès lors, le diabétologue joue un rôle crucial dans le dépistage, la coordination des soins et l’ajustement des thérapeutiques diabétologiques.
Résumé
La gastroparésie diabétique, définie par un retard de la vidange de l’estomac sans obstruction mécanique, revêt un spectre clinique très vaste. Le rôle du diabétologue y est primordial dans son dépistage, notamment au regard de certaines situations glycémiques et, plus largement, dans la coordination des soins avec les gastroentérologue, nutritionniste, psychologue. Après confirmation du diagnostic et évaluation du traitement spécifique des éventuels symptômes, il conviendra également d’adapter le traitement du diabète, en particulier l’insulinothérapie avec, le plus souvent, l’aide de la mesure continue du glucose. Même si les résultats doivent être confirmés, les dernières données publiées de l’utilisation des systèmes automatisés d’insulinothérapie sont prometteuses.
Abstract
Diabetic gastroparesis: diabetological perspectives
Diabetic gastroparesis, which is characterised by delayed gastric emptying without mechanical obstruction, exhibits a wide range of clinical manifestations. The endocrinologist plays a crucial role in screening for it, particularly in relation to certain blood glucose profiles, as well as coordinating care with the gastroenterologist, dietitian and psychologist. Once the diagnosis has been confirmed and specific treatment for any symptoms has been evaluated, it will also be necessary to adjust diabetes management, particularly insulin therapy, which is most often achieved with the use of continuous glucose monitoring. Although the results need to be confirmed, the latest published data on automated insulin therapy systems are promising.
Keywords: Diabetes, Gastroparesis, Continuous glucose monitoring, Treatment
Généralités
La gastroparésie, définie par un retard de vidange de l’estomac sans obstruction mécanique, affecte la qualité de vie et le contrôle glycémique des patients. Sa fréquence est estimée entre 30 et 50 % après 20 ans de diabète de type 1 ou 2 (DT1, DT2) (1). Sa physiopathologie demeure complexe avec, pour principaux protagonistes, la neuropathie autonome, des troubles de la coordination antro-pyloro-duodenale, une dysfonction des neurones nitrergiques « nNos » avec pylorospasme, une désorganisation des cellules de Cajal avec anomalies de propagation des contractions, et une hypocontractibilité musculaire en lien avec le stress oxydant et l’hyperglycémie (2).
Souvent sous-diagnostiquée, son spectre clinique est très large, le rôle du diabétologue est donc crucial dans le dépistage, la prise en charge multidisciplinaire et l’ajustement du traitement du diabète.
Suspecter et reconnaître la gastroparésie
Schématiquement, la suspicion de gastroparésie repose sur des symptômes soit glycémiques, soit digestifs, voire les deux.
Les symptômes glycémiques
Tout d’abord, s’agissant de l’équilibre glycémique, il faut rappeler que la vidange gastrique rend compte d’environ 35 % de la variance glycémique post-prandiale, ainsi, l’instabilité glycémique constitue une situation très fréquente de diagnostic de gastroparésie, surtout dans le DT1, moins dans le DT2 (1). Cette instabilité glycémique se caractérise par des hypoglycémies précoces après la prise alimentaire, antérieurement dénommées “hypoglycémies gastriques”, plus ou moins associées à des situations d’hyperglycémies retardées par rapport à la prise alimentaire, parfois nocturnes. La mesure continue du glucose (MCG), très largement utilisée aujourd’hui, facilite l’identification de ces situations. Il faut y ajouter l’analyse attentive de la délivrance d’insuline des systèmes automatisés. En effet, l’arrêt de la pompe en situation post-prandiale précoce peut résulter d’un retard de vidange gastrique après avoir écarté un surdosage du bolus prandial (Fig. 1).
L’étude de Lupoli et al. (3) rapporte une vidange gastrique ralentie chez 36 % des patients vivant avec un DT1, avec une durée moyenne de la maladie de 19 ans sans complication diabétique connue et totalement asymptomatique, ce qui soulève la question de l’intérêt d’un dépistage actif et davantage systématique des anomalies de la vidange gastrique, notamment en cas d’instabilité du contrôle glycémique post-prandial (3).
Les symptômes digestifs
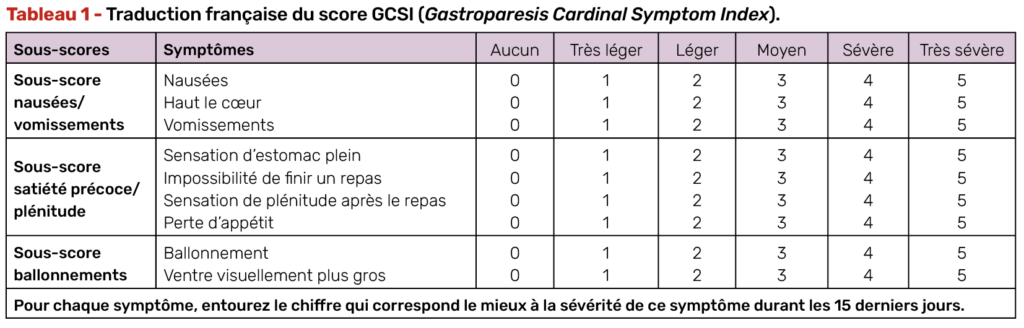
S’agissant des symptômes digestifs, il est important de mener un interrogatoire précis sur cette problématique, car le lien entre diabète et troubles digestifs n’est pas toujours évident pour les patients. À l’heure actuelle, le questionnaire Gastroparesis Cardinal Symptom Index (GCSI) (Tab. 1) peut être utilisé pour suivre les malades, la diminution de 1 point de ce score allant de 0 à 5 étant souvent considérée comme témoin d’une amélioration symptomatique.
Avant d’envisager les examens complémentaires pour confirmer la gastroparésie, il convient d’écarter la prise de médicaments responsables de ralentissement de vidange gastrique tels que les médicaments opioïdes, les agonistes dopaminergiques, les antidépresseurs tricycliques ou les agonistes du GLP-1, ainsi que certains toxiques tels que le cannabis.
Coordonner la prise en charge multidisciplinaire
À partir de la suspicion clinique ou “glycémique” de gastroparésie, la poursuite des examens complémentaires peut être réalisée en concertation avec les médecins gastroentérologues.
Les examens complémentaires
Il s’agit tout d’abord d’effectuer une mesure de la vidange gastrique :
• soit par un test de vidange gastrique isotopique (gold standard, anormale si taux de rétention des solides > 10 % à la 4e heure),
• soit par la méthode breath test, non irradiant, avec un repas marqué au carbone 13.
Considérant que l’hyperglycémie aiguë est reconnue pour induire un ralentissement de la vidange gastrique, il faudra s’assurer que le test de mesure de vidange soit réalisé avec une glycémie basale inférieure à 10 mmol/l, ainsi, un protocole d’insulinothérapie adapté peut être proposé en concertation avec les gastroentérologues.
En outre, dans les examens complémentaires, une endoscopie haute des voies digestives sera recommandée afin d’écarter tout obstacle mécanique (2, 4).
Les pistes thérapeutiques
En cas de diagnostic avéré, plusieurs pistes thérapeutiques sont à explorer.
La prise en charge diététique
En premier lieu, une prise en charge diététique est sollicitée systématiquement (4). Il s’agit de favoriser les boissons liquides, de limiter les graisses, les fibres, les sodas et les boissons alcoolisées. Fractionner les repas peut également être utile.
La prise en charge médicamenteuse
En cas de vomissements sévères, plusieurs options médicamenteuses peuvent être discutées toujours en concertation multidisciplinaire, en rappelant néanmoins qu’à ce jour nulle molécule n’a obtenu l’AMM dans l’indication de gastroparésie.
• L’érythromycine, agoniste des récepteurs de la motiline, en cure courte intraveineuse, est souvent prescrite en première ligne avec surveillance rapprochée de l’espace QT de l’ECG et les possibles interactions médicamenteuses de l’ordonnance du patient. La prescription au long cours n’est pas recommandée compte tenu d’un phénomène de tachyphylaxie.
• D’autres molécules prokinétiques, telles que la dompéridone ou les agonistes 5HT4, peuvent être envisagées toujours en cure courte avec la surveillance des effets indésirables spécifiques.
• Des molécules antiémétiques, telles que les antagonistes dopaminergiques, les antagonistes 5HT3, voire les antagonistes NK1, et d’autres traitements médicamenteux en cours d’études déjà décrits (5), sont aussi discutées.
Les autres techniques
• Dans les situations cliniques sévères, une prise en charge nutritionnelle, avec possible jéjunostomie, peut s’avérer nécessaire.
• En outre, de nouvelles prises en charge endoscopiques sont aujourd’hui disponibles telles que l’injection intrapylorique de toxine botulinique pour lever le pylorospasme et, plus récemment, le GPOEM (Gastric Per Oral Endoscopic Myotomy). Cette dernière technique, qui consiste à disséquer les fibres musculaires pyloriques par voie sous-muqueuse, a montré une efficacité significative sur l’amélioration du score GCSI dans plusieurs essais randomisés (6).
• La pose d’un stimulateur gastrique peut constituer également une alternative thérapeutique. L’essai multicentrique français ENTERRA a démontré que le pacemaker gastrique réduisait significativement la fréquence des vomissements (7).
À ce jour, l’utilisation des différentes options thérapeutiques repose avant tout sur la disponibilité de la technique et l’expertise des centres. La coordination des soins entre les diabétologues, les gastroentérologues, les diététiciens ou nutritionnistes et parfois psychologues est importante afin de proposer une prise en charge optimale en fonction de la sévérité de la situation clinique.
Ajuster le traitement diabétique
Dans la situation de gastroparésie documentée, l’ajustement du traitement du diabète est important afin d’améliorer l’équilibre glycémique en réduisant notamment le risque d’hypoglycémie.
Écarter les molécules qui ralentissent la vidange gastrique
Dans le contexte de DT2, comme cela a déjà été mentionné, il faudra écarter les médications qui ralentissent la vidange gastrique telles que les analogues du GLP-1 ou les fortes doses de pramlintide (non commercialisé en France) et préférer des molécules neutres telles que les gliflozines. L’utilisation de la metformine doit être extrêmement prudente au regard des vomissements, du risque d’insuffisance rénale et d’acidose lactique. Le recours à une insulinothérapie peut se discuter dans les situations sévères avec vomissements et dénutrition.
Surveiller les profils glycémiques
L’ajustement du traitement insulinique et de sa surveillance constitue également une étape déterminante de la prise en charge. Tout d’abord, la MCG avec le paramétrage des alarmes paraît aujourd’hui un outil incontournable pour la surveillance de ces profils glycémiques très instables. Outre son intérêt pour le repérage d’une possible gastroparésie, cette surveillance permet d’adapter les modalités de l’insulinothérapie et de prévenir le risque d’hypoglycémie.
Adapter l’insulinothérapie
Si les essais randomisés restent encore aujourd’hui trop peu nombreux, les données les plus récentes orientent de plus en plus vers les systèmes d’infusion sous-cutanée continue, voire les systèmes automatisés d’insulinothérapie avec des paramétrages spécifiques.
Tout d’abord, le timing bolus doit être adapté à la gastroparésie, l’injection de l’insuline prandiale peut être conseillée au milieu ou la fin du repas. De la même façon, chez les patients traités avec certains modèles de pompe à insuline, il conviendra de réduire la vitesse du bolus. En effet, une étude de clamp glycémique a montré que la réalisation d’une injection d’insuline en 10 minutes versus 30 secondes permettait de décaler l’effet maximal de l’injection de 30 minutes (8). En outre, l’utilisation des analogues d’insuline ultrarapides sera plutôt déconseillée, car pourrait favoriser les hypoglycémies.
Une étude pilote menée par le NIDDK Gastroparesis Clinical Research Consortium (GpCRC) a évalué la sécurité et l’efficacité potentielle de l’infusion sous-cutanée continue d’insuline (CSII) combinée à la MCG chez 45 patients atteints de diabète mal contrôlé et de gastroparésie pendant 24 semaines (9). Les résultats objectivent une amélioration significative du time in range (TIR) de 44 à 52 % (p = 0,02), avec réduction du temps passé en hypoglycémie (3,9 versus 1,8 % ; p < 0,001). Le protocole de l’étude préconisait l’utilisation de bolus duo réalisés 10 minutes après le repas ou dès que la glycémie augmentait, 10 à 20 % du bolus en flash, 80 à 90 % sur 4 à 6 heures. L’utilisation des bolus duo est également associée à une amélioration de l’équilibre glycémique dans l’étude de Lee W et al. (10).
Des résultats prometteurs avec les boucles fermées
Les données obtenues avec les boucles fermées restent parcellaires, mais plutôt prometteuses. Plusieurs case reports relèvent des améliorations des paramètres de MCG, une augmentation du TIR moyen de 26 à 58 % chez sept patients analysés (11). Le paramétrage des systèmes automatisés peut être adapté à la gastroparésie en fonction des dispositifs et aux profils glycémiques : utilisation de bolus post-prandiaux étendus sur plusieurs heures, suppression des auto-bolus, augmentation de la durée de l’insuline active, ratio glucidique et cibles glycémiques moins stricts. Une récente étude française rapporte, chez cinq patients, une amélioration très significative des données de MCG, mais également des symptômes digestifs (questionnaire GCSI) parallèlement à l’amélioration de la vidange gastrique recontrôlée après 6 mois de boucle fermée (12).
Si ce résultat se confirmait sur de plus larges cohortes, les systèmes automatisés d’insuline pourraient constituer alors une option thérapeutique de choix dans le traitement de la gastroparésie et la place des traitements invasifs, tels que GPOEM ou pacemaker gastrique, pourrait alors être reconsidérée dans les algorithmes du traitement de la gastroparésie.
Gaëtan Prévost déclare avoir des liens d’intérêt (études cliniques et/ou consultant) avec Abbott, Amgen, Asten, AstraZeneca, Boehringer Ingelheim, Lilly, ISIS Diabete, Medtronic, Novartis, NovoNordisk, Sanofi et Guillaume Gourcerol avec Enterra, Medtronic et Dr Falk.
Bibliographie
1. Bharucha AE, Kudva YC, Prichard DO. Diabetic gastroparesis. Endocr Rev 2019 ; 40 : 1318‑52.
2. Phillips LK, Deane AM, Jones KL et al. Gastric emptying and glycaemia in health and diabetes mellitus. Nat Rev Endocrinol 2015 ; 11 : 112‑28.
3. Lupoli R, Pisano F, Capaldo B. postprandial glucose control in type 1 diabetes: importance of the gastric emptying rate. Nutrients 2019 ; 11 : 1559.
4. Schol J, Wauters L, Dickman R et al. United European Gastroenterology (UEG) and European Society for Neurogastroenterology and Motility (ESNM) consensus on gastroparesis. Neurogastroenterol Motil 2021 ; 33 : e14237.
5. Fontaine S. La gastroparésie diabétique : nouvelles promesses thérapeutiques Diab Obes 2024 ; 19 : 63-8.
6. Martinek J, Hustak R, Mares J et al. Endoscopic pyloromyotomy for the treatment of severe and refractory gastroparesis: a pilot, randomised, sham-controlled trial. Gut 2022 ; 71 : 2170‑8.
7. Ducrotte P, Coffin B, Bonaz B et al. Gastric electrical stimulation reduces refractory vomiting in a randomized crossover trial. Gastroenterology 2020 ; 158 : 506-14.
8. Regittnig W, Urschitz M, Lehki B et al. Insulin bolus administration in insulin pump therapy: effect of bolus delivery speed on insulin absorption from subcutaneous tissue. Diabetes Technol Ther 2019 ; 21 : 44‑50.
9. Calles-Escandón J, Koch KL, Hasler WL et al. Glucose sensor-augmented continuous subcutaneous insulin infusion in patients with diabetic gastroparesis: An open-label pilot prospective study. PLoS One 2018 ; 13 : e0194759.
10. Lee SW, Cao M, Sajid S et al. The dual-wave bolus feature in continuous subcutaneous insulin infusion pumps controls prolonged post-prandial hyperglycaemia better than standard bolus in Type 1 diabetes. Diabetes Nutr Metab 2004 ; 17 : 211‑6.
11. Daly A, Hartnell S, Boughton CK, Evans M. Hybrid closed-loop to manage gastroparesis in people with type 1 diabetes: a case series. J Diabetes Sci Technol 2021 ; 15 : 1216‑23.
12. Phan F, Halbron M, Jacqueminet S et al. Improved dyspeptic symptoms of type 1 diabetes adults with gastroparesis on hybrid closed loop system: A case series. Diabetes Metab 2023 ; 49 : 101471.