Résumé
La maladie stéatosique du foie liée à une dysfonction métabolique (MASLD) est actuellement la première cause de maladie hépatique au monde. Elle est susceptible d’évoluer vers des stades plus sévères incluant la stéatohépatite liée à une dysfonction métabolique (MASH) et la fibrose hépatique. Ces stades, bien que longtemps asymptomatiques, ont une incidence forte sur le pronostic des patients et nécessite une prise en charge spécialisée. Le traitement de la MASH a classiquement consisté en l’utilisation de médicaments hépatoprotecteurs tels que la vitamine E et l’acide ursodéoxycholique limités en termes d’efficacité ou de sécurité. Une nouvelle approche thérapeutique par le resmétirom, un agoniste sélectif ciblant le foie et agissant sur le récepteur THR-β, est désormais possible. Son efficacité, démontrée dans des essais cliniques récents, avec des résultats significatifs sur la résolution de la MASH et l’amélioration de la fibrose hépatique, a conduit à son approbation par la Food and Drug Administration (FDA) dernièrement. D’autres traitements prometteurs sont en cours de développement, et permettront de consolider les options thérapeutiques pour les patients atteints de MASH dans le futur. Dans l’attente de la commercialisation de ces traitements en France, certains traitements anti-diabétiques ont démontré des effets bénéfiques hépatiques et peuvent être privilégiés chez les patients avec diabète de type 2 et MASLD en association avec la prise en charge nutritionnelle par modification du mode de vie.
Abstract
Metabolic dysfunction-related fatty liver disease: new therapeutic approaches
Metabolic dysfunction-related fatty liver disease (MASLD) is currently the leading cause of chronic liver disease worldwide. MASLD can progress towards metabolic dysfunction-related steatohepatitis (MASH) and liver fibrosis. These stages, although asymptomatic for a long time, have a strong impact on the prognosis of patients and require specialized care. Treatment of MASH has traditionally consisted of the use of hepatoprotective drugs such as vitamin E and ursodeoxycholic acid, which are limited in terms of effectiveness or safety. A new approach is the treatment with resmetirom, a selective agonist targeting the liver and acting on THR-β receptor. Its efficacy has been demonstrated in recent clinical trials, with significant improvement on MASH resolution and liver fibrosis leading to the recent approval by the Food and Drug Administration (FDA). Other promising molecules are under development for the treatment of MASH and have the potential to consolidate therapeutic options for patients with MASH in the future. While we are expected these new treatments in France, certain anti-diabetic treatments have demonstrated beneficial hepatic effects and can be favored in patients with type 2 diabetes and MASLD in association with nutritional management and lifestyle intervention.
Introduction
Définition
La stéatose hépatique non alcoolique (NAFLD) a récemment été renommée la maladie stéatosique du foie liée à une dysfonction métabolique (MASLD, Metabolic dysfunction–Associated Liver Disease) (1). Cette nouvelle nomenclature a renforcé le rôle des facteurs cardio-métaboliques qui désormais rentrent dans la définition de la maladie tels que la présence d’une dyslipidémie, un surpoids, une hypertension ou la présence d’un diabète de type 2 (DT2) ou une intolérance au glucose (1).
Les patients à risque
Certains groupes de patients sont particulièrement à risque de MASLD et de progression vers des formes sévères telles que la stéatohépatite liée à une dysfonction métabolique (MASH) ou la fibrose avancée correspondant aux stades histologiques F3 et F4. La présence d’une fibrose hépatique est associée à une augmentation du risque de mortalité globale en particulier cardiovasculaire, de morbi-mortalité hépatique et de transplantation hépatique. Il existe actuellement un fort consensus concernant la nécessité d’évaluer le statut hépatique des patients à risque afin d’identifier ceux atteints de fibrose avancée.
Cette évaluation hépatique devrait s’intégrer dans l’évaluation annuelle des comorbidités associées au DT2 et permettra de mieux prendre en charge ces patients présentant de multiples comorbidités métaboliques.
Stratégie thérapeutique
L’évaluation hépatique des patients à risque de MASLD est actuellement renforcée par l’approbation très récente en mars 2024 du resmétirom comme le premier traitement dans l’indication de la MASH par le Food and Drug Administration (FDA). Cette approbation apporte la perspective de nouvelles approches pharmacologiques pour le traitement de la MASLD dont bénéficieront largement les patients atteints de DT2 et d’obésité. Par ailleurs, si la modification du mode de vie et la perte de poids demeurent une stratégie efficace pour améliorer tous les stades de la MASLD, d’autres approches pharmacologiques peuvent être envisagées pour améliorer le statut hépatique des patients souffrant de maladies métaboliques comme le DT2 et l’obésité qui pourront compléter, voire remplacer, les traitements hépatoprotecteurs classiquement prescrits chez les patients atteints de MASH par les hépatologues (2, 3).
Les traitement médicamenteux “hépatoprotecteurs” classiquement utilisés chez les patients atteints de MASH
La vitamine E
L’une des voies physiopathologiques de la MASH implique le stress oxydatif, ainsi la vitamine E comme anti-oxydant peut être efficace pour le traitement de la MASH. L’efficacité du traitement par vitamine E a été démontrée dans l’essai contrôlé randomisé PIVENS (pioglitazone, vitamine E ou placebo pour la stéatohépatite non alcoolique) avec une amélioration des lésions de MASH significativement plus élevée chez les sujets traités par vitamine E à forte dose versus placebo, mais sans amélioration des lésions de fibrose hépatique. Par la suite, plusieurs autres études ont démontré un effet bénéfique hépatique, également confirmé par une méta-analyse incluant huit essais et démontrant que la vitamine E réduit les valeurs des enzymes hépatiques par rapport au placebo, et améliore de manière statistiquement significative les lésions histologiques de MASH. Néanmoins, le traitement par vitamine E à forte dose au long cours a été associé à une augmentation de la mortalité toutes causes de manière dose-dépendante et à un risque plus élevé d’AVC hémorragique et de cancer de la prostate.
La vitamine E demeure hors AMM dans l’indication de la MASH, mais elle est recommandée par l’American Association for the Study of Liver Diseases (AASLD) 2023 pour les adultes non diabétiques atteints de MASH confirmée par biopsie, bien que les bénéfices et les risques doivent être discutés avec chaque patient (4). En revanche, son utilisation n’est pas recommandée pour les patients diabétiques, ceux atteints de cirrhose liée à la MASH, ou ceux sans biopsie hépatique (4).
L’acide ursodéoxycholique (AUDC)
L’AUDC est un acide biliaire naturel possédant plusieurs activités hépatoprotectrices : il réduit le stress oxydatif et a des effets anti-apoptotiques. L’AUDC a été beaucoup utilisé en routine pour le traitement de la MASH, et a été assez largement évalué. Une revue systématique de 12 essais contrôlés randomisés a conclu que l’AUDC est efficace contre la MASH, en particulier lorsqu’il est associé à d’autres médicaments, surtout des anti-oxydants, comme la vitamine E. Cependant, la plupart des études étaient de faible qualité avec une grande hétérogénéité.
En l’absence de données robustes confirmant un effet bénéfique sur les lésions de MASH ou de fibrose hépatique, l’AUCD n’est pas recommandé pour le traitement de la MASH (4, 5).
Les nouveaux traitements efficaces de la MASH
Le resmétirom
Le resmétirom est un agoniste sélectif oral ciblant le foie et agissant sur le récepteur thyrotropin-releasing hormone–β (THR-β). Le récepteur THR-β est impliqué dans la modulation du métabolisme lipidique hépatique qui est souvent altérée chez les patients atteints de MASH (6). En effet, ils ont des niveaux réduits d’activité hormonale thyroïdienne hépatique, ce qui entraîne une fonction hépatique altérée.
Depuis le 14 mars 2024, le resmétirom (Rezdiffra®) est le premier traitement approuvé dans l’indication de la MASH par la FDA.
Résultats
Cette approbation fait suite aux résultats positifs de l’essai clinique contrôlé randomisé en double aveugle versus placebo : MAESTRO-NASH. Dans cet essai clinique de phase III, la sécurité et l’efficacité du resmétirom ont été évaluées lors d’une analyse intermédiaire après 12 mois de traitement chez des patients atteints de MASH avec un stade de fibrose F2 ou F3. Au total, 966 patients ont constitué la population d’analyse principale (322 dans le groupe resmétirom de 80 mg, 323 dans le groupe resmétirom de 100 mg et 321 dans le groupe placebo). La résolution de la MASH sans aggravation de la fibrose a été atteinte chez 25,9 % des patients du groupe resmétirom 80 mg et chez 29,9 % de ceux du groupe resmétirom 100 mg, comparé à 9,7 % pour le groupe placebo (p < 0,001 pour les deux comparaisons versus placebo). Une amélioration de la fibrose d’au moins un stade sans aggravation du score d’activité de la MASH a été obtenue chez 24,2 % des patients du groupe resmétirom 80 mg et chez 25,9 % de ceux du groupe resmétirom 100 mg, comparé à 14,2 % de ceux du groupe placebo (p < 0,001 pour les deux comparaisons versus placebo).
Profil de tolérance, mises en garde et précautions
Le profil de tolérance du resmétirom est également rassurant, les effets secondaires les plus courants sous traitement sont les diarrhées et les nausées.
Le traitement par resmétirom est accompagné de certaines mises en garde et précautions, en particulier un risque faible de toxicité hépatique médicamenteuse. De plus, l’utilisation de resmétirom doit être évitée chez les patients atteints de cirrhose décompensée. Enfin, certaines précautions d’usage sont notifiées concernant l’interaction avec d’autres traitements, en particulier avec les statines.
Sur la base de ces données, la FDA a donc approuvé le resmétirom dans le cadre du processus d’approbation accélérée, qui permet une approbation rapide des médicaments traitant des affections graves et répondant à un besoin médical non satisfait, sur la base d’un critère de substitution ou d’intermédiaire clinique raisonnablement susceptible de prédire un bénéfice clinique, dans ce cas, l’amélioration des lésions histologiques de MASH ou fibrose hépatique. Cette approbation sera maintenue à condition de démontrer un effet bénéfique du resmétirom sur la survenue d’événements cliniques hépatiques comparé au placebo. Ainsi, l’essai clinique se poursuit actuellement pour une durée totale de 54 mois.
Autres traitements actuellement étudiés pour le traitement de la MASH
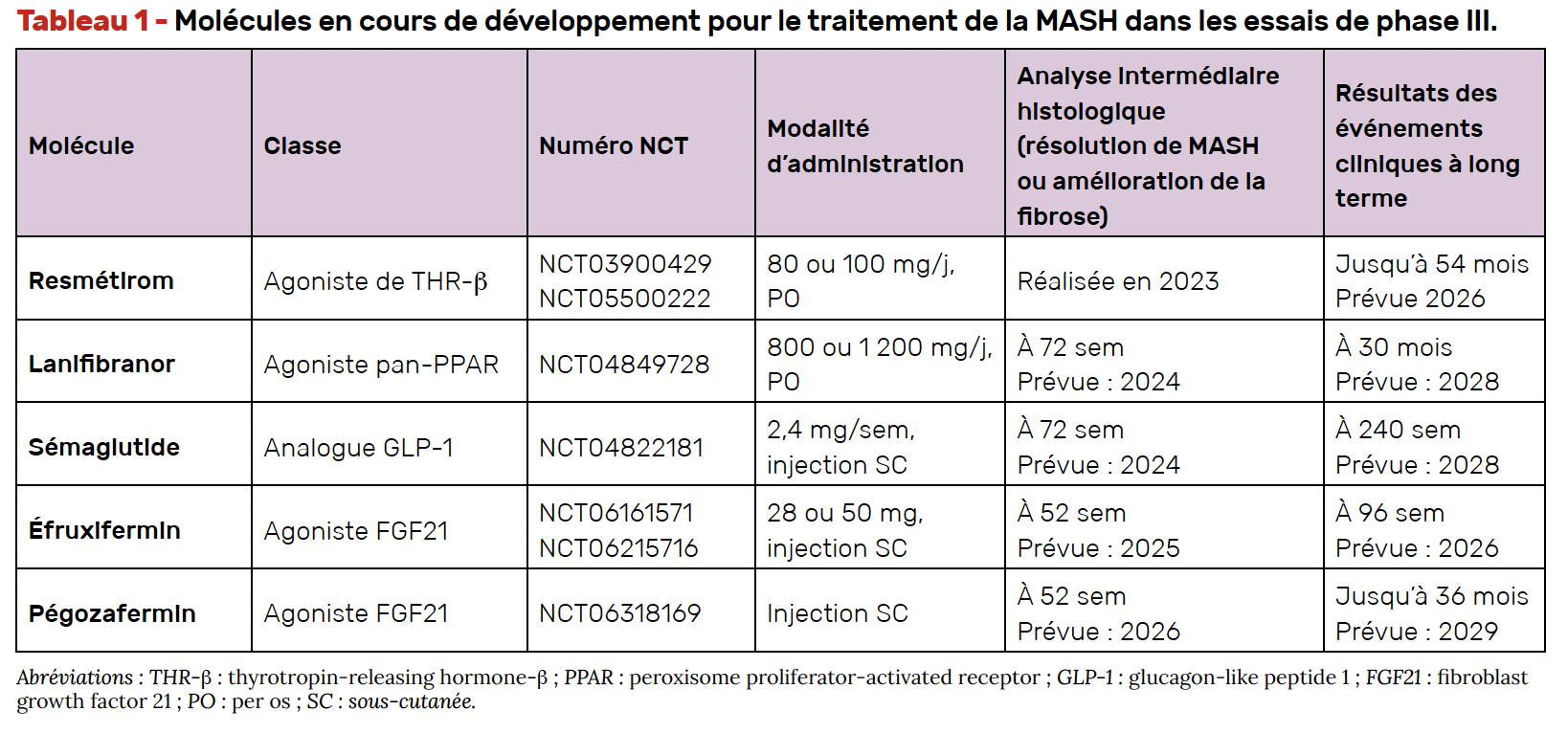
De nombreuses autres molécules sont en cours de développement pour le traitement de la MASH et avec différents mécanismes d’action (7). Les molécules les plus avancées dans leur programme de développement et actuellement étudiées dans le cadre d’essai clinique de phase III chez des patients atteints de MASH, sont résumées dans le tableau 1.
Le lanifibranor
Le lanifibranor est une petite molécule orale qui exerce une activité anti-fibrotique et anti-inflammatoire ainsi qu’un effet métabolique bénéfique sur l’organisme en activant chacune des trois isoformes du récepteur du peroxisome proliferator-activated (PPAR) : PPARα, PPARδ et PPARγ.
L’éfruxifermin et le pégozafermin
Deux analogues du récepteur du fibroblast growth factor 21 (FGF21), éfruxifermin et pégozafermin sont également étudiés. Le FGF21 est impliqué dans la régulation du métabolisme glucidique, lipidique et énergétique.
Le sémaglutide
Enfin, parmi ces molécules prometteuses, on retrouve le sémaglutide, un analogue du GLP-1, largement prescrit par les endocrinologues, les diabétologues et les nutritionnistes dans l’indication du DT2 à la dose de 1 mg par semaine et récemment approuvé à la dose de 2,4 mg par semaine pour le traitement de l’obésité. Actuellement, le sémaglutide fait l’objet d’une évaluation dans le cadre de l’essai clinique de phase III dont les premiers résultats d’analyse intermédiaire concernant la résolution de la MASH ou l’amélioration de la fibrose hépatique sont attendus fin 2024.
Effet bénéfique des traitements anti-diabétiques sur la MASLD
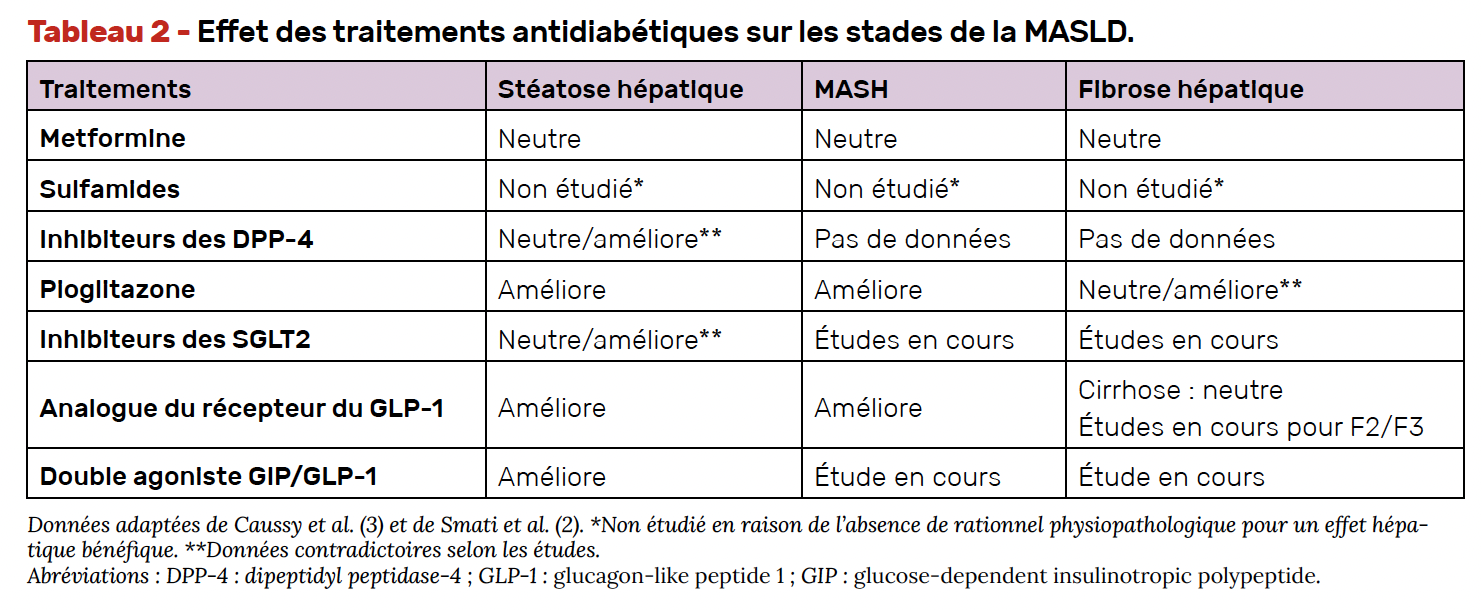
Le DT2 et la MASLD sont très fortement associés. La prévalence globale de la MASLD chez les patients atteints de DT2 est estimée à 55 % dans le monde et la prévalence estimée de la MASLD chez les patients avec DT2 atteint environ 68 % en Europe (8). Ces deux pathologies partagent des mécanismes physiopathologiques communs notamment l’insulino-résistance. À l’instar du sémaglutide, les effets d’autres traitements anti-diabétiques, en particulier améliorant l’insulino-résistance, ont donc été logiquement étudiés chez les patients atteints de MASLD avec ou sans diabète. La synthèse des effets hépatiques des traitements anti-diabétiques sur les histologiques de la MASLD comprenant la stéatose hépatique, la MASH et la fibrose est résumée dans le tableau 2 et détaillée ci-après (2, 3).
La metformine
Plusieurs essais cliniques randomisés ont étudié l’effet de la metformine sur la MASLD. Dans l’ensemble, ces essais n’ont pas réussi à démontrer une amélioration significative de la stéatose hépatique, de la MASH ou de la fibrose hépatique.
Par conséquent, la metformine n’est pas recommandée à l’heure actuelle pour le traitement de la MASLD (4, 5).
La pioglitazone
La pioglitazone, un agoniste des récepteurs PPARγ, diminue la résistance à l’insuline, réduit la lipotoxicité hépatique et favorise le stockage des lipides dans le tissu adipeux sous-cutané.
Bien que l’essai PIVEN n’ait pas montré d’amélioration significative de la MASH, une dose plus élevée de pioglitazone (45 mg/jour) a été associée à une résolution significative de la MASH chez les patients atteints de pré-diabète ou de DT2. Plusieurs essais cliniques et une méta-analyse ont confirmé ces bénéfices pour la MASH et la stéatose hépatique. En revanche, l’effet de la pioglitazone sur l’amélioration de la fibrose hépatique est moins clair, car des résultats contradictoires sont rapportés dans les essais cliniques. Néanmoins, une autre méta-analyse récente regroupant huit essais cliniques randomisés suggère que la pioglitazone pourrait améliorer la fibrose hépatique avancée (stade F3 ou F4) chez les patients avec et sans DT2.
Les recommandations actuelles de l’AASLD et de l’EASL soutiennent l’utilisation de la pioglitazone chez les patients diabétiques atteints de MASH confirmée par biopsie. Bien que retiré du marché français en 2011 en raison de préoccupations concernant le cancer de la vessie, ce traitement reste disponible dans de nombreux pays dans le monde, ces inquiétudes n’ont pas été confirmées par la suite. Récemment, l’American Association of Clinical Endocrinology (AACE) a également recommandé le traitement par pioglitazone chez les patients DT2 atteints de MASH (9).
Les inhibiteurs de la DPP-4
Peu d’essais cliniques randomisés ont étudié l’effet des inhibiteurs de la DPP-4 sur la MASLD. Ils ont principalement évalué son incidence sur la stéatose hépatique. Une première avait démontré que la sitagliptine était sûre, mais n’avait pas d’efficacité supérieure au placebo pour l’amélioration de la stéatose hépatique chez les patients atteints de pré-diabète ou de DT2 et de MASLD. D’autres études sont contradictoires et ont rapporté une diminution significative de la stéatose hépatique chez les patients atteints de DT2 traités par la vildagliptine comparé à un traitement placebo après 6 mois de traitement.
À ce jour, il n’y a pas eu d’études ni de données disponibles concernant un éventuel effet des inhibiteurs de DPP-4 sur les lésions de MASH ou de fibrose hépatique.
Les inhibiteurs de SGLT2
Les inhibiteurs de SGLT2 induisent de multiples changements métaboliques bénéfiques, notamment par la modification de l’utilisation de substrats métaboliques qui favorise la cétogenèse hépatique et l’utilisation accrue des acides gras hépatiques non estérifiés.
Des études cliniques ont rapporté une réduction des concentrations plasmatiques des enzymes hépatiques médiée principalement par la perte de poids et un meilleur contrôle glycémique. De plus, des essais cliniques ont rapporté une diminution de la teneur en graisses hépatiques sous empagliflozine, dapagliflozine et la licogliflozine.
En raison de leur effet bénéfique sur la protection cardiovasculaire, rénale et l’homéostasie glucidique, les inhibiteurs du SGLT2 pourraient avoir un intérêt chez les patients atteints de MASH. En revanche, pour l’instant, leur effet sur l’amélioration histologique de la MASH ou de la fibrose hépatique n’est pas connu en l’absence de données pour lesquelles des études sont en cours (2, 3).
Les analogues du GLP-1
Les effets hépatiques des GLP-1 ont été largement étudiés. Bien qu’il n’y ait pas d’action directe du GLP-1 sur le foie, une action indirecte a été montrée via la perte de poids ou l’amélioration du métabolisme globale avec des actions indirectes médiées par le tissu adipeux.
Le liraglutide
• Dans l’étude LIRA-NAFLD, le traitement par liraglutide (Victoza®) pendant 6 mois chez des patients atteints de DT2 non contrôlé a démontré une réduction de poids et une réduction significative de la graisse hépatique de 31 % évaluée par spectroscopie par résonance magnétique.
• La méta-analyse réalisée par Armstrong et al. à partir des données individuelles de plus de 4 000 patients atteints de DT2 inclus dans des essais cliniques pour le développement de liraglutide, a rapporté une réduction significative des enzymes hépatiques sous liraglutide 1,8 mg par jour comparé au placebo.
• Bien que ce résultat ait été principalement médié par la perte de poids et le contrôle glycémique, ces données préliminaires ont conduit au développement de l’essai clinique LEAN, un essai de phase II multicentrique, randomisé en double aveugle contrôlé par placebo incluant 52 patients atteints de MASH avec et sans diabète (10). L’étude LEAN a démontré une résolution histologique significativement plus importante de la MASH sans aggravation de la fibrose chez les patients traités par liraglutide 1,8 mg par jour versus placebo.
Le sémaglutide
• Enfin, très récemment, une deuxième étude de phase II de plus grande ampleur incluant 320 patients traités par sémaglutide 0,1, 0,2 ou 0,4 mg par jour versus placebo (soit des doses différentes du sémaglutide 1 mg (Ozempic®) par semaine disponible pour le traitement du DT2) a été publiée. Elle confirme un effet bénéfique du sémaglutide sur la MASH avec une proportion significativement plus importante de participants avec une résolution de la MASH sous sémaglutide 0,4 mg/j (59 %) versus placebo (17 %) (11). En revanche, cette étude n’a pas démontré de réduction significative de la fibrose hépatique comparé au bras placebo.
• Par ailleurs, l’effet du sémaglutide 2,4 mg hebdomadaire versus placebo a également été étudié dans un essai clinique randomisé en double aveugle de phase II chez des sujets atteints de cirrhose liée à la MASH à un stade compensé pendant 48 semaines. Cette étude n’a pas montré d’amélioration significative de la fibrose hépatique ou de la MASH sous sémaglutide 2,4 mg hebdomadaire comparé au groupe placebo (12). Néanmoins, cette étude a permis de démontrer un profil de tolérance satisfaisant sans effets indésirables hépatiques ou rénaux du traitement par sémaglutide 2,4 mg par semaine dans cette population, les principaux effets secondaires étaient ceux habituellement observés sous analogues du GLP-1 (nausées, diarrhées, vomissements) (12).
Pour les sujets sans cirrhose, il faudra donc attendre les résultats de l’essai de phase III ESSENCE pour une éventuelle indication pour le traitement de la MASH. Cependant, le traitement par sémaglutide peut être considéré chez les patients atteints de MASH dans le cadre de ses indications approuvées, i.e. DT2 et/ou obésité, d’après les recommandations de l’AASLD 2023 (4) et de l’AACE (9).
Les double agonistes GIP/GLP-1
Le tirzépatide, un double agoniste du GLP-1 et du peptide insulinotrope dépendant du glucose (GIP), a récemment obtenu une AMM européenne pour le traitement du DT2 et de l’obésité. Il a également démontré une amélioration de la MASLD.
• Dans une sous-étude de SURPASS-3, une diminution relative du contenu en graisse intra-hépatique de 39 % sous tirzépatide 15 mg hebdomadaire (mesurée par imagerie par résonance magnétique) a été rapportée après 52 semaine de traitement (13).
• De plus, des résultats positifs de l’essai de phase II SYNERGY (NCT04166773), étudiant l’efficacité et la tolérance du tirzépatide chez des patients atteints de MASH versus placebo, ont été annoncés très récemment.
Il s’agit donc d’un traitement potentiellement intéressant pour le traitement de la MASH qui sera très probablement étudié dans un essai de phase 3.
Conclusion
Les nouvelles approches pharmacologiques pour le traitement de la MASH vont permettre de traiter efficacement les patients qui présentent souvent de multiples comorbidités métaboliques. Le resmétriom est le premier traitement approuvé dans l’indication de la MASH, mais de nombreuses autres molécules prometteuses sont en cours de développement et permettront de renforcer l’arsenal thérapeutique et les options thérapeutiques en fonction du profil des patients à l’avenir. Compte tenu de la complexité de la physiopathologie de la MASLD associant de multiples voies de régulation, l’association de molécules avec des modes d’action complémentaires sera probablement nécessaire pour améliorer l’effet de ces thérapeutiques et permettre une efficacité durable, bien entendu accompagnée de modification du mode de vie pour un meilleur équilibre nutritionnel.
Il apparaît donc plus que jamais nécessaire d’évaluer le statut hépatique des patients DT2 et atteints d’obésité qui sont les plus à risque de développer des formes sévères de la MASLD telles que la MASH ou la fibrose hépatique, car ils pourront largement bénéficier de ces innovations thérapeutiques. Enfin, en attendant la disponibilité de ces traitements, une optimisation des traitements anti-diabétiques en privilégiant ceux avec un bénéfice hépatique est possible chez les patients atteints de DT2 et MASLD.
Cyrielle Caussy déclare avoir des liens d’intérêt avec NovoNordisk, Gilead, AstraZeneca, E-scopics, Bayer, Lilly, Ipsen, MSD, Gilead, Echosens.
Bibliographie
1. Rinella ME, Lazarus JV, Ratziu V et al. A multisociety Delphi consensus statement on new fatty liver disease nomenclature. Hepatology 2023 ; 78 : 1966-86.
2. Smati S, Canivet CM, Boursier J et al. Anti-diabetic drugs and NASH: from current options to promising perspectives. Expert Opin Investig Drugs 2021 ; 30 : 813-25.
3. Caussy C, Aubin A, Loomba R. The Relationship between type 2 diabetes, NAFLD, and cardiovascular risk. Curr Diab Rep 2021 ; 21 : 15.
4. Rinella ME, Neuschwander-Tetri BA, Siddiqui MS et al. AASLD Practice Guidance on the clinical assessment and management of nonalcoholic fatty liver disease. Hepatology 2023 ; 77 : 1797-35.
5. EASL-EASD-EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver disease. J Hepatol 2016 ; 64 : 1388-402.
6. Harrison SA, Bedossa P, Guy CD et al. A Phase 3, randomized, controlled trial of resmetirom in NASH with liver fibrosis. N Engl J Med 2024 ; 390 : 497-509.
7. Harrison SA, Loomba R, Dubourg J et al. Clinical trial landscape in NASH. Clin Gastroenterol Hepatol 2023 ; 21 : 2001-14.
8. Younossi ZM, Golabi P, de Avila L et al. The global epidemiology of NAFLD and NASH in patients with type 2 diabetes: A systematic review and meta-analysis. J Hepatol 2019 ; 71 : 793-801.
9. Cusi K, Isaacs S, Barb D et al. American Association of clinical endocrinology clinical practice guideline for the diagnosis and management of nonalcoholic fatty liver disease in primary care and endocrinology clinical settings: co-sponsored by the American association for the study of liver diseases (AASLD). Endocr Pract 2022 ; 28 : 528-62.
10. Armstrong MJ, Gaunt P, Aithal GP et al. Liraglutide safety and efficacy in patients with non-alcoholic steatohepatitis (LEAN): a multicentre, double-blind, randomised, placebo-controlled phase 2 study. Lancet 2016 ; 387 : 679-90.
11. Newsome PN, Buchholtz K, Cusi K et al. A placebo-controlled trial of subcutaneous semaglutide in nonalcoholic steatohepatitis. N Engl J Med 2021 ; 384 : 1113-24.
12. Loomba R, Abdelmalek MF, Armstrong MJ et al. Semaglutide 2.4 mg once weekly in patients with non-alcoholic steatohepatitis-related cirrhosis: a randomised, placebo-controlled phase 2 trial. Lancet Gastroenterol Hepatol 2023 ; 8 : 511-22.
13. Gastaldelli A, Cusi K, Fernandez Lando L et al. Effect of tirzepatide versus insulin degludec on liver fat content and abdominal adipose tissue in people with type 2 diabetes (SURPASS-3 MRI): a substudy of the randomised, open-label, parallel-group, phase 3 SURPASS-3 trial. Lancet Diabetes Endocrinol 2022 ; 10 : 393-406.