La prise en charge du diabète des personnes âgées est d’une grande actualité en raison de l’augmentation conjointe de la prévalence de la maladie et de l’espérance de vie. C’est ainsi qu’à ce jour un patient diabétique sur quatre est âgé de plus de 75 ans. La plupart de ces malades présente un diabète de type 2, mais aujourd’hui beaucoup de personnes atteignent un âge avancé en dépit de leur diabète de type 1. L’amélioration de la qualité des soins chez ces nombreuses personnes diabétiques est donc une priorité afin d’éviter les complications et de majorer leur espérance de vie en bonne santé. Afin de parvenir à ces objectifs, il est nécessaire d’observer une conduite précise et coordonnée pour adapter leur prise en charge.
Résumé
La prévalence du diabète chez les personnes âgées augmente régulièrement en raison de l’élévation de l’espérance de vie. La prise en charge de ces malades nécessite d’intégrer l’optimisation de l’équilibre glycémique et des facteurs de risque cardiovasculaire, mais également de prendre en compte les aspects gériatriques de la maladie. Cette démarche passe par une adaptation des objectifs thérapeutiques et des traitements en évitant la polymédication, source d’accidents iatrogènes.
Abstract
Elderly patients living with diabetes: How can their care be improved?
The prevalence of diabetes among older people is steadily increasing due to rising life expectancy. The management of these patients requires optimizing glycemic control and cardiovascular risk factors, but also taking into account the geriatric aspects of the disease. This goal requires adapting therapeutic objectives and treatments, avoiding polypharmacy, which can lead to iatrogenic accidents.
Repérer les malades fragiles
L’évaluation de la présentation clinique des patients diabétiques âgés est indispensable et constitue le premier élément qui permettra ensuite de déterminer les risques encourus, les objectifs thérapeutiques et les traitements à mettre en œuvre.
Cette démarche consiste idéalement en une évaluation gérontologique standardisée, mais, dans la pratique, l’objectif est d’intégrer le malade dans l’une de ces trois catégories :
• patient en bonne santé,
• patient fragile,
• patient à la santé très altérée
avec de nombreux outils comme les critères de Linda Fried ou le score de fragilité clinique (1, 2).
Évaluer le risque cardiovasculaire et rénal
La détermination du risque cardiovasculaire et rénal s’inscrit dans ce contexte, car il conditionne les objectifs et oriente le mode de traitement.
L’évaluation du risque cardiovasculaire
L’évaluation du risque cardiovasculaire repose sur différents outils adaptés à l’âge des personnes diabétiques.
• L’échelle SCORE2-Diabète 2 inclut dans ses paramètres la notion de diabète, mais n’est applicable qu’entre 40 et 69 ans.
• En revanche, le SCORE2-OP (Old Person) concerne les sujets de plus de 70 ans et évalue le risque à 10 ans d’événement cardiovasculaire fatal ou non fatal (IDM, AVC) mais n’intègre pas le diabète (3).
• Le score PREVENT, développé par l’American Heart Association (AHA) précise le risque des maladies cardiovasculaires sur une période de 10 et 30 ans, y compris, l’insuffisance cardiaque et s’applique aux adultes âgés de 30 à 79 ans. Il prend en compte la présence d’un diabète et également l’augmentation du risque cardiovasculaire liée à la maladie rénale chronique (MRC) (4).
L’évaluation de la maladie rénale chronique
L’évaluation de la MRC est également essentielle dans la précision de l’état clinique de la personne à la fois sur le plan du risque cardiovasculaire et sur celui de la progression vers l’insuffisance rénale terminale. Elle se définit par la diminution pendant plus de 3 mois du débit de filtration glomérulaire estimé (DFGe) en dessous de 60 ml/mn/1,73 m² et/ou par une élévation du rapport albuminurie sur créatininurie (RAC) mesurée à deux reprises sur un simple échantillon d’urine lorsqu’elle est supérieure ou égale à 30 mg/g ou 3 mg/mmol.
Le score de risque rénal (SRR) ou score KFRE (Kidney Failure Risk Equation) est un outil validé intégrant le DFGe et le RAC qui permet d’estimer le risque de progression vers une insuffisance rénale terminale (5).
Adapter les objectifs glycémiques
L’HbA1c
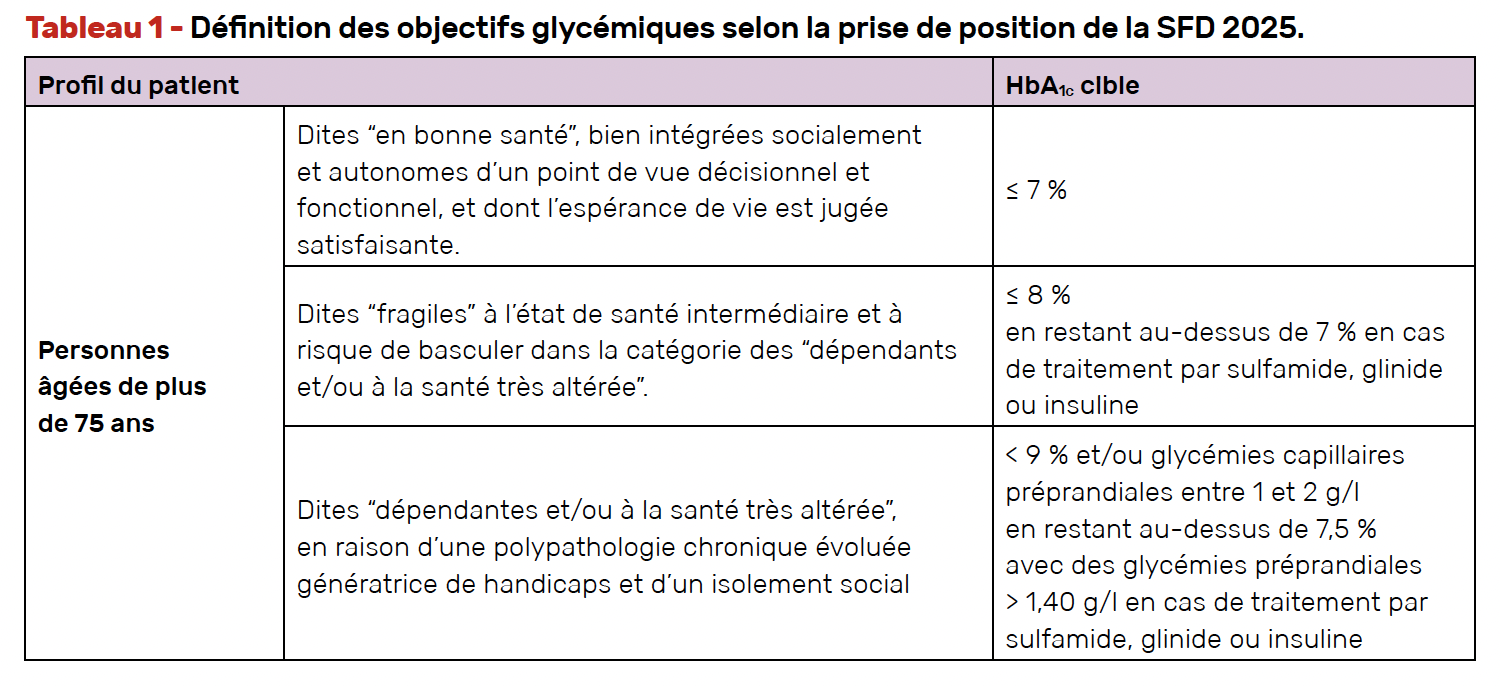
La dernière prise de position de la SFD publiée à la fin de l’année 2025 consacre un chapitre important aux objectifs glycémiques fondés sur le niveau de l’HbA1c et adaptés à la présentation clinique de la personne (Tab. 1) (6).
• Chez les patients “en bonne santé”, la cible d’HbA1c est ≤ 7 %.
• Chez les patients “fragiles”, elle est ≤ 8 % en restant au-dessus de 7 % en cas de traitement pouvant induire des hypoglycémies. D’ailleurs, les sulfamides hypoglycémiants ou les glinides sont à éviter dans ce contexte de fragilité.
• Chez les patients “dépendants et/ou à la santé très altérée”, l’objectif de l’HbA1c est < 9 % et/ou celui des glycémies capillaires préprandiales entre 1 et 2 g/l en restant au-dessus de 7,5 % et/ou des glycémies préprandiales > 1,40 g/l en cas de traitement par sulfamides hypoglycémiants, glinides ou insuline.
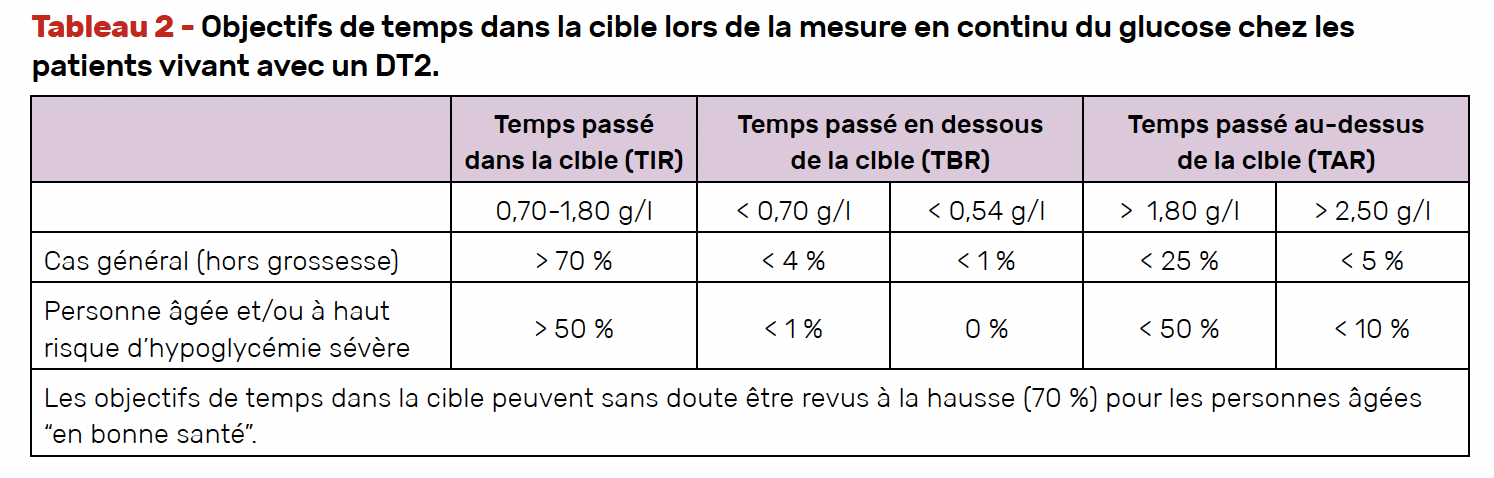
La mesure en continu du glucose
La mesure en continu du glucose (CGM) a pour intérêt de préciser les objectifs glycémiques et de mettre en évidence des épisodes d’hypoglycémies qui resteraient méconnus. Chez les personnes âgées fragiles, ces objectifs sont moins ambitieux que chez les personnes plus jeunes et visent à prévenir les hypoglycémies sévères notamment nocturnes (Tab. 2) (7). Malheureusement, dans les Ehpad, la prise en charge des dispositifs médicaux et donc du CGM entre dans le cadre du forfait soin qui est relativement faible (environ 3 € par jour et par patient), si bien que certains établissements refusent de financer l’achat des capteurs pour les malades qui en auraient pourtant besoin.
Éviter les hypoglycémies
Les hypoglycémies ne sont pas rares en cas de traitement par sulfamide, glinide ou insuline. Ainsi, dans l’étude HYPOAGE, menée avec une CGM durant 28 jours chez des patients âgés en moyenne de plus de 80 ans, et traités par insuline, plus de la moitié des participants a présenté des périodes d’hypoglycémie nocturne < 54 mg/dl pendant plus de 15 minutes consécutives entre minuit et 6 h du matin (8). Cette fréquence s’explique par le caractère souvent silencieux ou la présentation atypique de la symptomatologie comportant notamment des troubles du comportement ou une agressivité (9).
Facteurs favorisants
Les circonstances favorisantes de ces accidents sont multiples et multifactorielles, associant notamment :
• des objectifs glycémiques trop stricts,
• un traitement à risque mal maîtrisé,
• une alimentation irrégulière
• et des altérations cognitives.
Complications
Les hypoglycémies, surtout lorsqu’elles sont sévères, entraînent des conséquences importantes sur le plan des complications cardiovasculaires et gériatriques comme les chutes ou les troubles cognitifs.
Lutter contre les facteurs de risque cardiovasculaire et infectieux
Un âge supérieur à 75 ans ne doit pas faire négliger la prise en charge des facteurs de risque cardiovasculaire comme la pression artérielle et le niveau de la cholestérolémie, mais aussi la nécessité d’obtenir une couverture vaccinale optimale.
L’hypertension artérielle
La prise en charge de l’hypertension artérielle (HTA) est essentielle afin de réduire les accidents cardiovasculaires et notamment les AVC, mais aussi les complications microangiopathiques et la mortalité.
Les dernières recommandations ont ainsi défini les objectifs de pression artérielle :
• pour les patients de 64 à 79 ans : moins de 140/80 mmHg, voire moins de 130/80 mmHg si le traitement est bien toléré sans aller en dessous de 120/70 mmHg ;
• pour les patients de plus de 80 ans, la prudence consiste à débuter par une monothérapie et de majorer le traitement progressivement sans dépasser trois antihypertenseurs. Chez les patients fragiles, l’initiation de la thérapeutique est nécessaire à partir d’une PAS ≥ 160 mmHg avec un objectif tensionnel situé entre 140 et 150 mmHg sans hypotension orthostatique afin d’éviter les chutes (10).
La dyslipidémie
L’intérêt du traitement d’une dyslipidémie doit être nuancé chez les personnes âgées. En prévention primaire, il n’y a pas d’indication à initier la prescription de ces médicaments après 70 ans, mais la poursuite de ce traitement, s’il est bien supporté, peut se justifier en cas de risque cardiovasculaire élevé. Enfin, chez les patients âgés de plus de 75 ans, l’effet bénéfique des statines en prévention secondaire est bien démontré (10).
Les vaccins
L’amélioration de la qualité de la couverture vaccinale est indispensable, puisque la pathologie infectieuse constitue la troisième cause de mortalité pour l’ensemble de la population et que certaines infections peuvent être couvertes par la vaccination. Les vaccins permettent ainsi d’éviter la survenue ou de limiter les conséquences de nombreuses affections comme la grippe, la Covid-19, les pneumococcies, la coqueluche, le VRS et le zona.
En dépit de ces évidences, la couverture vaccinale reste insuffisante tout particulièrement chez les malades à risque comme ceux vivant avec un diabète (11).
Éviter les complications gériatriques
Les complications plus spécifiquement gériatriques s’intègrent avec celles du diabète. Leur dépistage et leur prise en charge sont donc particulièrement importants (12).
Les troubles cognitifs
Les troubles cognitifs, allant de l’altération cognitive modérée (mild cognitive impairment) à la démence, ne sont pas rares chez les personnes âgées vivant avec un diabète (13). La maladie d’Alzheimer est un peu plus fréquente au cours du diabète, mais ce sont les démences vasculaires qui sont le plus souvent observées avec une prévalence multipliée par un facteur deux à trois en raison de la majoration du risque d’AVC au cours du diabète (14).
Le dépistage des troubles cognitifs ainsi que celui des syndromes dépressifs est indispensable afin d’adapter le mode de prise en charge de ces malades.
Les chutes
La survenue de chutes constitue fréquemment un tournant évolutif dans l’histoire de la personne diabétique âgée. Les causes sont très diverses comme les complications iatrogènes (hypotension orthostatique et hypoglycémies), mais peuvent être également la conséquence d’une sarcopénie, d’une neuropathie ou de troubles du rythme cardiaque.
Le risque de chute doit être systématiquement évalué par une étude de la marche, de la station unipodale et du lever de chaise. En effet, les chutes sont souvent responsables de fractures en raison de l’existence d’une ostéoporose et peuvent induire une appréhension à la reprise de la marche.
La dénutrition
La dénutrition, qui comporte très souvent un degré de sarcopénie, constitue un facteur aggravant de la qualité de vie des personnes et imprime un effet négatif au pronostic. Ses causes sont multiples et intriquées, liées à la dépression, à la perte du goût ou de l’odorat et aux troubles bucco-dentaires (15).
La dénutrition doit être systématiquement dépistée, prévenue et prise en charge par une alimentation équilibrée et adaptée aux préférences du patient. Les régimes diabétiques et restrictifs doivent être bannis.
Adapter la stratégie thérapeutique
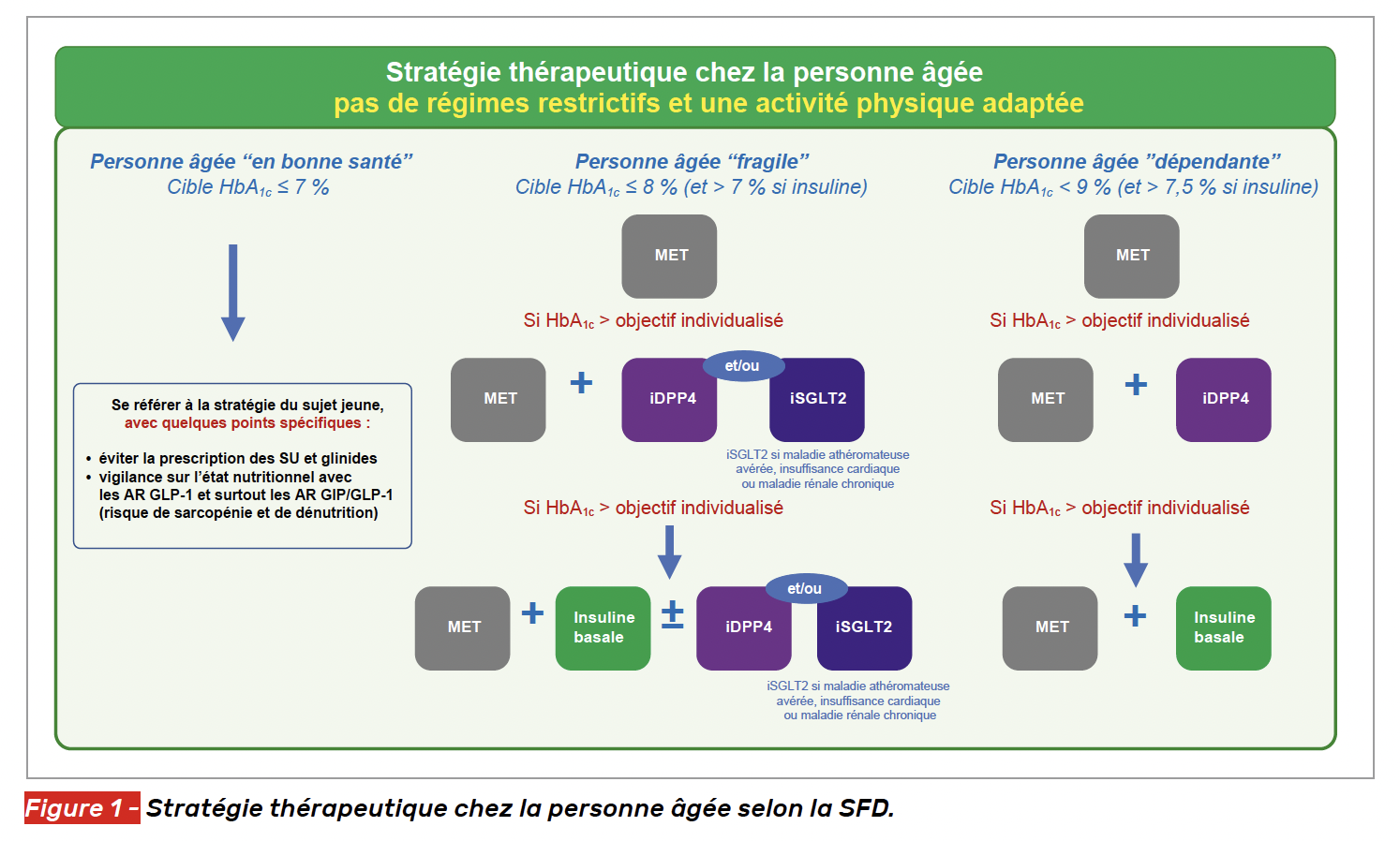
La stratégie thérapeutique de la prise en charge de l’hyperglycémie chez les sujets âgés a été précisée dans les dernières recommandations de la SFD, qui prennent particulièrement en compte la présentation clinique des malades (Fig. 1) (6).
Dans tous les cas, une alimentation régulière et variée sans régime strict en dehors de la prise à jeun de sucres rapides et une activité physique adaptée sont recommandées.
Chez les personnes en “bonne santé”
Chez les personnes “en bonne santé” qui ont bien vieilli, le mode de traitement est voisin de celui des sujets jeunes en évitant la prescription des sulfamides et des glinides en raison du risque hypoglycémique et en exerçant une vigilance particulière avec les AR GLP-1, source possible de dénutrition.
Chez les personnes “fragiles” ou “dépendantes”
Pour les personnes “fragiles” ou “dépendantes”, l’utilisation de la metformine en l’absence d’insuffisance rénale sévère et d’une gliptine est privilégiée tandis que le recours à une insulinothérapie basale est souvent nécessaire. La prescription d’un iSGLT2 se justifie en cas d’insuffisance cardiaque ou de maladie rénale chronique.
Lutter contre la polymédication et favoriser la déprescription
La détermination des différents objectifs permet d’adapter les traitements, d’éviter la polymédication et d’engager si nécessaire une procédure de déprescription.
• La polymédication se définit par l’utilisation de cinq médicaments ou plus pendant au moins 6 mois, situation particulièrement fréquente chez les personnes âgées diabétiques en raison de la multiplicité des affections. Ce fait, favorisé par l’utilisation des ordonnances enregistrées, peut entraîner des problèmes de sécurité des prises, mais également des interactions médicamenteuses et d’importants risques iatrogènes.
• L’éducation thérapeutique devrait permettre aux malades ou aux aidants de connaître le rôle de chaque médicament, d’améliorer l’adhésion au traitement et d’éviter l’automédication.
• La décroissance thérapeutique concerne l’ensemble des soignants et nécessite leur formation. Le principal critère pour la poursuite ou non d’un médicament devrait être le rapport bénéfice/risque sans attendre les effets indésirables, en particulier, lorsque les résultats dépassent les objectifs.
Le pharmacien devrait jouer un rôle important dans cette démarche en prenant en compte la parapharmacie et en consultant régulièrement le dossier pharmaceutique.
Bernard Bauduceau déclare avoir réalisé des interventions ponctuelles pour les entreprises Abbott, AstraZeneca, Merck Sharp & Dohme, Novartis, Novo Nordisk, Boehringer Ingelheim, GSK, Bristol-Myers Squibb, Pfizer, Sanofi, Eli Lilly.
Lyse Bordier déclare avoir réalisé des interventions ponctuelles pour les entreprises Adelia, AstraZeneca, Bayer, Merck Sharp & Dohme, Novartis, Novo Nordisk, Sanofi, Eli Lilly, Boehringer Ingelheim, Bristol-Myers Squibb, Servier, Becton Dickinson, Jansen.
Bibliographie
1. Fried LP, Tangen CM, Walston J et al. Frailty in older adults: evidence for a phenotype. J Gerontol A Biol Sci Med Sci 2001 ; 56 : M146-56.
2. Rockwood K, Song X, MacKnight C et al. A global clinical measure of fitness and frailty in elderly people. CMAJ 2005 ; 173 : 489-95.
3. SCORE2-OP working group and ESC Cardiovascular risk collaboration. SCORE2-OP risk prediction algorithms: estimating incident cardiovascular event risk in older persons in four geographical risk regions. Eur Heart J 2021 ; 42 : 2455-67.
4. Khan SS, Coresh J, Pencina MJ et al. Novel prediction equations for absolute risk assessment of total cardiovascular disease incorporating cardiovascular-kidney-metabolic health: a scientific statement from the American Heart Association. Circulation 2023 ; 148 : 1982-2004.
5. Tangri N, Stevens AS, Griffith J et al. A predictive model for progression of chronic kidney disease to kidney failure. JAMA 2011 ; 305 : 1553-9.
6. Darmon P, Bauduceau B, Bordier L et al. Prise de position de la Société francophone du diabète (SFD) sur les stratégies d’utilisation des traitements de l’hyperglycémie dans le diabète de type 2 – 2025. Med Mal Metab 2025 ; 19 : 630-62.
7. Joubert M, Bouillet B, Prevost G et al. Prise de position d’un groupe d’experts – Utilisation de la mesure en continu du glucose chez les patients vivant avec un diabète de type 2 en France. Med Mal Metab 2025 ; 19 : 331-47.
8. Boureau AS, Guyomarch B, Gourdy P et al. Nocturnal hypoglycemia is underdiagnosed in older people with insulin-treated type 2 diabetes: The HYPOAGE observational study. J Am Geriatr Soc 2023 ; 71 : 2107-19.
9. Bauduceau B, Bordier L. Les hypoglycémies chez les diabétiques âgés : fréquentes, graves et sous-estimées. Diabétol Prat 2015 ; 50 : 10-1.
10. Benetos A, Bauduceau B. Prise en charge des facteurs de risque cardiovasculaire des personnes âgées de 75 ans et plus. Bull Acad Natl Med 2025 ; 209 : 480-96.
11. Bauduceau B, Sultan A. La couverture vaccinale : un enjeu de santé publique pour la prévention des infections chez les personnes vivant avec un diabète. Med Mal Metab 2025 ; 20 : 42-6.
12. Vischer UM, Bauduceau B, Bourdel-Marchasson I et al. A call to incorporate the prévention and treatment of geriatric disorders in the management of diabetes in the elderly. Diabetes Metab 2009 ; 35 : 168-77.
13. de Broqueville G, Hanon O, Buysschaert M, Boland B. Déficiences cognitives et démences des patients diabétiques âgés. Med Mal Metab 2023 ; 17 : 8S25-31.
14. Bauduceau B, Bordier L, Le Floch JP et al. Les troubles cognitifs chez les patients diabétiques âgés. Apport de l’étude Gérodiab. Bull Acad. Natle Méd 2016 ; 200 : 859-75.
15. Haute Autorité de Santé (HAS). Fédération Française de Nutrition (FFN). Diagnostic de la dénutrition chez la personne de 70 ans et plus. Recommandations pour la pratique clinique. Recommandation. 10 novembre 2021. Disponible sur : www.has-sante.fr/jcms/p_3165944/fr/diagnostic-de-la-denutrition-chez-la-personne-de-70-ans-et-plus.